
工业上合成氨在一定条件下进行如下反应:N2(g)+3H2(g)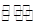 2NH3(g) △H=-92.44
kJ/mol。其部分工艺流程如下图所示:
2NH3(g) △H=-92.44
kJ/mol。其部分工艺流程如下图所示:
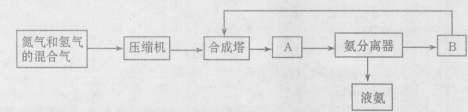
(1)合成氨所需要的原料气中,氮气取自 ,氢气来源于 。
(2)对原料气进行净化处理的目的是 。
(3)设备A的名称是 ,设备B的名称是 。
(4)在20~50 Mpa时,工业合成氨选择在400—500℃的温度进行反应,
主要原因是 。
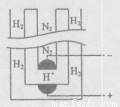
(5)据《科学》杂志报道,希腊化学家在常压下将氢气和用氢气稀释的氮气分别通人一个加热到570℃的电解池(如图)中,氢和氮在电极上合成了氨,且转化率达到了78%。则:阳极反应为 ,阴极反应为 。
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| 高温高压 |
| ||
| 高温高压 |
 CO(g)+3H2(g);△H=+QkJ/mol(Q>0)
CO(g)+3H2(g);△H=+QkJ/mol(Q>0)| 时间/min | CH4(mol) | H20( mol) | CO (mol) | H2 (mol) |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | X1 | X2 | X3 | 0.60 |
| 7 | Y1 | Y2 | 0.20 | Y3 |
| 10 | 0.21 | 0.81 | 0.19 | 0.62 |
查看答案和解析>>
科目:高中化学 来源:浙江省兰溪一中2010-2011学年高二下学期期中考试化学试题 题型:022
合成氨对化学工业和国防工业具有重要意义.
(1)
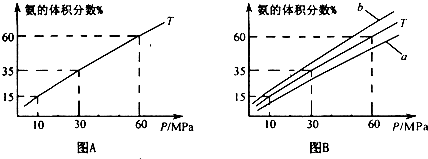
向合成塔中按1∶4的物质的量之比充入N2、H2进行氨的合成,图A为T℃时平衡混合物中氨气的体积分数与压强(P)的关系图.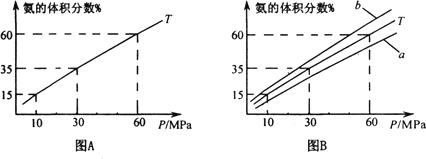
①写出工业上合成氨的化学方程式________.
②图
A中氨气的体积分数为15.00%时,H2的转化率=________.③图B中T=
500℃,温度为450℃对应的曲线是________(选填字母“a"或“b”),选择的理由是________.④由图像知,增大压强可提高原料的利用率,从生产实际考虑增大压强需解决的问题是________(写出一条即可).
(2)
合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为:![]()
(3)
一定温度下,在2 L容器中发生上述反应,各物质的物质的量变化如下表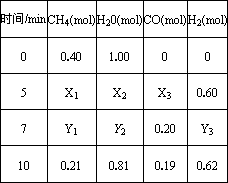
①分析表中数据,判断5~7
min之间反应是否处于平衡状态________(填“是”或“否”),前5 min平均反应速率v(CH4)=________.②反应在7~10
min之间,CO的物质的量减少的原因可能是________(填字母).a.
减少CH4b.
降低温度c.
增大压强d.
充入H2③
若保持温度不变,向1 L容器中起始充入0.15 mol CH4.0.45 mol H2O.________mol CO、________mol H2,达到平衡时CH4的体积百分含量与第一次投料相同.查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
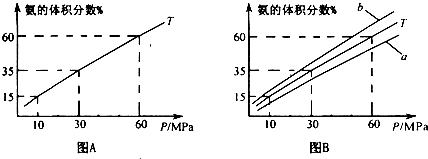

| 时间/min | CH4(mol) | H20( mol) | CO (mol) | H2 (mol) |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | X1 | X2 | X3 | 0.60 |
| 7 | Y1 | Y2 | 0.20 | Y3 |
| 10 | 0.21 | 0.81 | 0.19 | 0.62 |
查看答案和解析>>
科目:高中化学 来源:2010-2011学年浙江省金华市兰溪一中高二(下)期中化学试卷(解析版) 题型:填空题

 CO(g)+3H2(g);△H=+QkJ/mol(Q>0)
CO(g)+3H2(g);△H=+QkJ/mol(Q>0)| 时间/min | CH4(mol) | H20( mol) | CO (mol) | H2 (mol) |
| 0.40 | 1.00 | |||
| 5 | X1 | X2 | X3 | 0.60 |
| 7 | Y1 | Y2 | 0.20 | Y3 |
| 10 | 0.21 | 0.81 | 0.19 | 0.62 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(15 分)
合成氨对化学工业和国防工业具有重要意义。
(1) 向合成塔中按1:4的物质的量之比充入N2、H2进行氨的合成,图A为T0C时平衡混合物中氨气的体积分数与压强(P)的关系图。
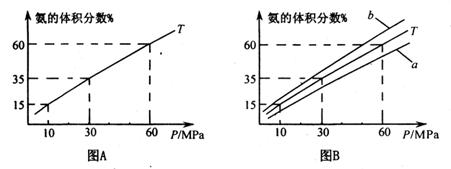
①写出工业上合成氨的化学方程式_____________________。
②图A中氨气的体积分数为15.00%时,H2的转化率=_______ 。
③图B中T=5000C,温度为4500C对应的曲线是_______(选填字母“a"或“b ”),选择的理由是______________
④由图像知,增大压强可提高原料的利用率,从生产实际考虑增大压强需解决的问题是_______(写出一条即可)。
(2) 合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为:
![]()
(3) 一定温度下,在2 L容器中发生上述反应,各物质的物质的量变化如下表
| 时间/min | CH4(mol) | H20( mol) | CO (mol) | H2 (mol) |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | X1 | X2 | X3 | 0.60 |
| 7 | Y1 | Y2 | 0.20 | Y3 |
| 10 | 0.21 | 0.81 | 0.19 | 0.62 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com