
分析 (1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,常见反应为氯气和氢氧化钠的反应;
(2)若A为紫红色金属,则A为Cu,D为红棕色气体,则D为NO2,应是Cu与浓硝酸反应生成硝酸铜、二氧化氮与水;
(3)若A为不含金属元素的盐,B为碱,应是铵盐与碱反应生成氨气,则气体C为氨气;
(4)若C、D均为气体且都能使澄清石灰水变浑浊,二者分别为SO2、CO2,为碳和浓硫酸的反应.
解答 解:(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,常见反应为氯气和氢氧化钠的反应,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(2)若A为紫红色金属,则A为Cu,D为红棕色气体,则D为NO2,应是Cu与浓硝酸反应生成硝酸铜、二氧化氮与水,反应方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑++2H2O,
故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑++2H2O;
(3)若A为不含金属元素的盐,B为碱,应是铵盐与碱反应生成氨气,则气体C为氨气,检验氨气的方法为:用湿润的红色石蕊试纸检验,若试纸变蓝,则说明为氨气,
故答案为:用湿润的红色石蕊试纸检验,若试纸变蓝,则说明为氨气;
(4)若C、D均为气体且都能使澄清石灰水变浑浊,二者分别为SO2、CO2,为碳和浓硫酸的反应,
故答案为:碳和浓硫酸.
点评 本题考查无机物的推断,把握元素化合物知识及物质的性质为解答的关键,注意利用题干信息及物质转化推断无机物,题目难度中等.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 不断补充氮气和氢气 | |
| B. | 选择20MPa-50MPa的高压 | |
| C. | 及时液化分离氨气 | |
| D. | 选择500℃左右的高温同时使用铁触媒做催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 合理使用药物是保证身心健康、提高生活质量的有效手段.药物化学已经成为化学的一个重要领域.
合理使用药物是保证身心健康、提高生活质量的有效手段.药物化学已经成为化学的一个重要领域. 是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为:
是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为:
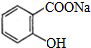 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ② | B. | ②④ | C. | ①③④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2溶液【FeCl3】:加足量铁粉 | B. | NaCl溶液【Na2SO4】:用Ba(OH)2溶液 | ||
| C. | Na2CO3固体【NaHCO3】:加热 | D. | 铁粉【铝粉】:用NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
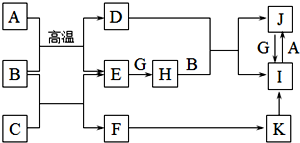
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为稀硫酸能与铁反应放出H2,所以稀硝酸与铁反应也一定能放出H2 | |
| B. | 因为Mg可以与水反应放出H2,所以Ca也可以与水反应放出H2 | |
| C. | 因为CO2的水溶液可以导电,所以CO2是电解质 | |
| D. | 因为SO2可以使酸性KMnO4溶液褪色,所以SO2具有漂白性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com