
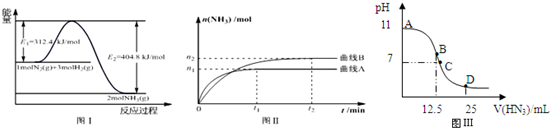
| �¶�/�� | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
���� ��1����֪����N2��g��+O2��g���T2NO��g����H1
��N2��g��+3H2��g��?2NH3��g����H2
��2H2��g��+O2��g���T2H2O��g����H3
���ݸ�˹���ɣ��ۡ�3-�١�2-�ڡ�2�ɵã�4NO��g��+4NH3��g��+O2��g���T4N2��g��+6H2O��g����
��2���٢�A����Ӧ�ʱ��H=312.4KJ/mol-404.8KJ/mol=-92.4kJ/mol��
B��ʹ�ô������ͷ�Ӧ�Ļ�ܣ�
C���¶�Խ��ƽ��������У���ҵ�����з�Ӧ������������Ч�ʺ;���Ч��ͣ�
D�����ȹ���ƽѹǿ����ѹǿpA��pB ������ѹǿƽ�������ƶ����������ʵ�������
E��ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ��䣬ƽ�ⳣ�����䣻
F������v=$\frac{��c}{��t}$����v��NH3��������������֮�ȵ��ڻ�ѧ������֮�ȼ���v��N2����
�ڿ��淴Ӧ����ƽ��ʱ��ͬ�����ʵ�������������ұ��ֲ��䣬����ֵ�Ũ�ȡ��������ֲ��䣬�ɴ�����������һЩ�����䣬�ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����ٱ仯˵������ƽ�⣻
��3���ɱ������ݿ�֪�����¶�����ƽ�ⳣ����С��˵������ӦΪ���ȷ�Ӧ��
��Ϊ������ƽ��ʱH2��ת���ʣ�Ӧ�ı�����ʹƽ�������ƶ���
�ڼ����ʱŨ����Qc����Qc=K������ƽ��״̬����Qc��K����Ӧ������Ӧ���У���Qc��K����Ӧ���淴Ӧ���У�
��4����ʼΪ��ˮ��Һ������ˮ�ĵ��룬B�����HN3��Һ���Ϊ12.5mL��ǡ�÷�Ӧ�õ�NH4N3��Һ����Һ�Լ��ԣ�˵��HN3Ϊ���ᣬ���ټ���HN3��Һ��������ˮ�ĵ��룬��ǡ�÷�Ӧʱˮ�ĵ���̶����
D�����25mL HN3��Һ����ʱΪ��Ũ�ȵ�NH4N3��HN3�����Һ����Һ�����ԣ�˵��NH4+����ˮ��̶ȴ��ڵ�N3-ˮ��̶ȣ�
��5��ԭ�������������ԭ��Ӧ��������������õ��ӣ������ʷ�Ӧ�������ӽ��Ϊ笠����ӣ�
��� �⣺��1����֪����N2��g��+O2��g���T2NO��g����H1
��N2��g��+3H2��g��?2NH3��g����H2
��2H2��g��+O2��g���T2H2O��g����H3
���ݸ�˹���ɣ��ۡ�3-�١�2-�ڡ�2�ɵã�4NO��g��+4NH3��g��+O2��g���T4N2��g��+6H2O��g������
3��H3-2��H1-2��H2��
�ʴ�Ϊ��3��H3-2��H1-2��H2��
��2����A����ͼ��֪����Ӧ�ʱ��H=312.4KJ/mol-404.8KJ/mol=-92.4kJ/mol����A��ȷ��
B��ʹ�ô����ı䷴Ӧ;�������ͷ�Ӧ�Ļ��E1����B����
C����Ӧ�Ƿ��ȷ�Ӧ���¶�Խ��ƽ��������У����ԭ�������ʣ����¶ȹ��ͣ���Ӧ���ʼ���������Ч�ʺ;���Ч��ͣ���C����
D�����ȹ���ƽѹǿ����ѹǿpA��pB ������ѹǿƽ�������ƶ����������ʵ�������ͼ����ѹǿԽ�������ʵ���ԽС��������ʵ�ʣ���D����
E��ͼ���Dz�ͬѹǿ�·�Ӧ��ϵ�а������ʵ����뷴Ӧʱ���ϵͼ���¶Ȳ��䣬��ƽ�ⳣ�����䣬��KA=KB
����E����
F��v��NH3��=$\frac{\frac{{n}_{1}mol}{2L}}{{t}_{1}min}$=$\frac{{n}_{1}}{2{t}_{1}}$mol/��L��min��������֮�ȵ��ڻ�ѧ������֮�ȣ�v��N2��=$\frac{1}{2}$v��NH3��=$\frac{{n}_{1}}{4{t}_{1}}$mol/��L��min������F��ȷ��
��ѡ��AF��
��A��ƽ��ʱ�����ʵ�Ũ�ȹ�ϵ����ʼŨ�ȼ�ת�����йأ���һ�������仯ѧ������֮�ȣ���A����
B��Ӧ��3v����N2��=v����H2��ʱ��Ӧ����ƽ�⣬��B����
C���淴Ӧ���л���������ʵ�����С�����º�����ѹǿ��С����������ѹǿ���ֲ���ʱ����Ӧ����ƽ�⣬��C��ȷ��
D������������������䣬�����ݻ����䣬���������ܶ�Ϊ��ֵ����D����
��ѡ��C��
��3���ɱ������ݿ�֪�����¶�����ƽ�ⳣ����С��˵������ӦΪ���ȷ�Ӧ��
������ӦΪ���������С�ķ��ȷ�Ӧ��Ϊ������ƽ��ʱH2��ת���ʣ���������ѹǿ���ʵ�������ȡ���ʱ����������е�NH3��
�ʴ�Ϊ������ѹǿ���ʵ�������ȡ���ʱ����������е�NH3��
�ڴ�ʱŨ����Qc=$\frac{{3}^{2}}{2��{1}^{3}}$=4.5��K=0.5����Ӧ���淴Ӧ���У���v����N2����v����N2����
�ʴ�Ϊ������
��4����ʼΪ��ˮ��Һ������ˮ�ĵ��룬B�����HN3��Һ���Ϊ12.5mL��ǡ�÷�Ӧ�õ�NH4N3��Һ����Һ�Լ��ԣ�˵��HN3Ϊ���ᣬ���ټ���HN3��Һ��������ˮ�ĵ��룬��ǡ�÷�Ӧ��B���ˮ�ĵ���̶����
D�����25mL HN3��Һ����ʱΪ��Ũ�ȵ�NH4N3��HN3�����Һ����Һ�����ԣ�˵��NH4+����ˮ��̶ȴ��ڵ�N3-ˮ��̶ȣ���Ӧ������Ũ�ȴ�С��c��N3-����c��NH4+����c��H+����c��OH-����
�ʴ�Ϊ��B��c��N3-����c��NH4+����c��H+����c��OH-����
��5��ԭ�������������ԭ��Ӧ��������������õ��ӣ������ʷ�Ӧ�������ӽ��Ϊ笠����ӣ������缫��ӦʽΪ��N2+8H++6e-�T2NH4+��
�ʴ�Ϊ��N2+8H++6e-�T2NH4+��
���� ���⿼�黯ѧƽ�������Ӱ�����ء���ѧƽ��״̬�жϡ�ƽ�ⳣ��Ӧ�á���ѧƽ��ͼ��˹����Ӧ�á�����Ũ�ȴ�С�Ƚϡ�ԭ��صȣ��Ƕ�ѧ���ۺ������Ŀ��飬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ǿ������ʵ���������Һ�ĵ���������С | |
| B�� | ��Һ�뽺��ı����������������ЧӦ | |
| C�� | ��ͬ�����£����������������������ֱ���ȫȼ�գ����߷ų��������� | |
| D�� | Լ��6.02��1023��Na+��Na2O2Ͷ��ˮ�����1L��Һ��Na+�����ʵ���Ũ��Ϊ1mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
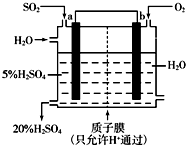 �����Ṥҵ�У�SO2ת��ΪSO3��һ���ؼ�����
�����Ṥҵ�У�SO2ת��ΪSO3��һ���ؼ�����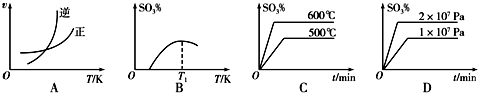
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����C02ͨ������������Һ�У�CO2+OH-�THCO3- | |
| B�� | Na202����H2180��2Na2O2+2H218O�T4Na++4OH-+18O2�� | |
| C�� | ���������ķ�Ӧ��Si+4H++4F-�TSiF4��+2H2�� | |
| D�� | ˮ������ͨ�˹���������̼��Na2SiO3+CO2+H2O�T2Na++CO32-+H2SiO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ�Ⱥ���ˮ��ͬһ���� | |
| B�� | ������������ȼ�ղ�����ɫ���� | |
| C�� | ������ˮ�ķ�Ӧ��������������ˮ�ǻ�ԭ�� | |
| D�� | ������Ư����Ϊ�˵õ��������Ư�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com