
【题目】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出现血红色。

(1)写出下列物质的化学式:A:_____;E:______。
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象:_______。
(3)按要求写方程式:B和R反应生成N的离子方程式:____________;M→W的离子方程式:________。
【答案】Na2O2 FeCl2 溶液中出现白色沉淀,在空气中迅速变成灰绿色,最终变成红褐色; ![]()
![]()
【解析】
A为淡黄色固体且能与水反应判断为Na2O2,D是具有磁性的黑色晶体判断为Fe3O4,C是无色无味的气体是过氧化钠与水反应生成的氧气,B为NaOH,W溶液中加入KSCN出现血红色,说明W含有三价铁离子;T、R为两种常见的用途很广的金属单质,T在C中燃烧生成D为四氧化三铁,溶于盐酸生成溶液中含有亚铁离子和三价铁离子,加入过量铁反应生成亚铁离子,证明T为Fe;E为FeCl2,H为Fe(OH)2,M为Fe(OH)3,W为FeCl3;金属R与B氢氧化钠反应说明R金属为Al,N为NaAlO2,Q为Al2O3;
(1)依据判断得到A、E的化学式分别为:A为 Na2O2,E为FeCl2,故答案为:Na2O2;FeCl2;
(2)B与E混和得到H为白色氢氧化亚铁沉淀,在潮湿空气中变成红褐色氢氧化铁沉淀的过程中,可能观察到的现象是:溶液中出现白色沉淀,在空气中迅速变成灰绿色,最终变成红褐色,故答案为:溶液中出现白色沉淀,在空气中迅速变成灰绿色,最终变成红褐色;
(3)B(NaOH)和R(Al)反应生成N(NaAlO2)的离子方程式为![]() ;M(Fe(OH)3)和盐酸反应生成W(FeCl3)反应的离子方程式为
;M(Fe(OH)3)和盐酸反应生成W(FeCl3)反应的离子方程式为![]() ;
;
故答案为:![]() ;
;![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知:pKa=-lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。用0.1 mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2SO3溶液的滴定曲线如图所示(曲线上的数字为pH)。下列说法正确的是( )

A.a点所得溶液中:2c(HSO3-)+c(SO32-)=0.1 mol/L
B.b点所得溶液中:c(H+)+c(SO32-)=c(OH-)+c(H2SO3)
C.c点所得溶液中:c(Na+)>3c(HSO3-)
D.d点所得溶液中:c(Na+)>c(OH-) >c(SO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象与结论对应关系正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 相同温度下,同时向 ①4 mL 0.1 molL-1 KMnO4酸性溶液和②4 mL 0.2 molL-1 KMnO4酸性溶液中,分别加入4 mL 1 molL-1 H2C2O4溶液 | ①中溶液先褪色 | 该实验条件下,KMnO4浓度越小,反应速率越快 |
B | 向煤炉中灼热的煤炭上洒少量水 | 产生淡蓝色火焰,煤炭燃烧更旺 | 加少量水后,可使煤炭燃烧放出更多的热量 |
C | 加热2NO2(g) | 颜色加深 | 证明正反应是放热反应 |
D | 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH | 后者较大 | 证明非金属性 S>C |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中加入过量Na2O2,有无色无味气体产生,同时有白色沉淀生成,其沉淀量与加入Na2O2的量的关系如图所示,由此确定,原溶液中含有的阳离子是( )
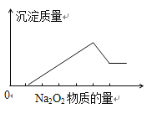
A.Mg2+、Al3+、Fe2+B.H+、Mg2+、Al3+C.H+、Ba2+、Al3+D.NH4+、Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气既是高效洁净的能源,又是重要的化工原料,在生产、生活中用途广泛。
(1)已知25℃、101kPa时,1 g甲烷不完全燃烧生成CO和液态水时放出37.96 kJ热量,则该条件下反应2CH4(g)+3O2(g)=2CO(g)+4H2O(l)的ΔH=______kJ·mol-1
(2)甲烷可以消除氮氧化物污染。如:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g)
N2(g)+CO2(g)+2H2O(g)
①下列措施能够使该反应速率加快的是______。
a.使用催化剂 b.降低温度 c.及时分离水
②若上述反应在恒容的密闭容器中进行,下列叙述中不能说明该反应已达平衡状态的是______。
a.容器内气体的压强不再变化 b.混合气体的质量不再变化
c.c(NO2) = 2c(N2) d.单位时间内生成1molCO2,同时生成2molNO2
(3)甲烷可直接应用于燃料电池,该电池采用可传导O2-的固体氧化物为电解质,其工作原理如图所示:
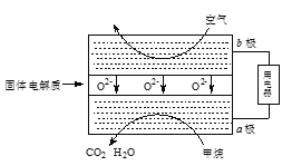
①外电路电子移动方向:____。(填“a极到b极”或“b极到a极”)。
②b极电极反应式为______。
③若燃料电池消耗的空气在标准状况下的体积是5.6L(假设空气中O2体积分数为20%),则理论上消耗甲烷______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有以下物质相互转化:
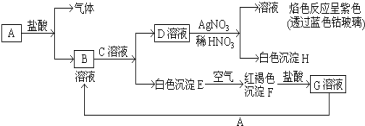
(1)写出下列各物质的化学式:
A___,B____,D___,F___,G___。
(2)写出由E转变成F的化学方程式___。
鉴别溶液G的试剂是__,现象___。
(3)G溶液和A反应的离子方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.NaHS在水中的电离方程式为NaHS=Na++HS﹣,HS﹣![]() H++S2﹣
H++S2﹣
B.氧化还原反应中,一种元素被氧化的同时必有另一种元素被还原
C.1mol配合物Fe(CO)5(羰基铁)中含有5mol配位键
D.氢氧化铁胶体带有正电荷,通电时向电源负极一端移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制备合成氨原料气过程中存在反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41kJ·mol-1,下列判断正确的是
CO2(g)+H2(g) △H=-41kJ·mol-1,下列判断正确的是
A. 该反应的逆反应是放热反应B. 反应物总能量小于生成物总能量
C. 反应中生成22.4LH2(g),放出41kJ热量D. 反应中消耗1mol CO(g),放出41kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应H2(g)+ ![]() O2(g)=H2O(g)的能量变化如图所示,a、b、c表示能量变化,为正值,单位为kJ,下列说法正确的是 ( )
O2(g)=H2O(g)的能量变化如图所示,a、b、c表示能量变化,为正值,单位为kJ,下列说法正确的是 ( )

A. H2(g)+ ![]() O2(g)=H2O(g) △H=c kJ·mol-1
O2(g)=H2O(g) △H=c kJ·mol-1
B. 2H2O(g)=2H2 (g)+O2 (g) △H=—2(a-b) kJ·mol-1
C. 1 mol氢气与0.5 mol氧气总能量为akJ
D. 2 mol氢气与1 mol氧气完全反应生成2 mol液态水放出的热量小于2(b-a)kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com