
【题目】一定条件下,下列各组物质能一步实现图中所示转化关系的是

选项 | X | Y | Z | W |
A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
B | Fe3O4 | Fe | FeCl2 | FeCl3 |
C | H2SO4 | SO2 | S | SO3 |
D | CH3CH2Br | CH2=CH2 | C2H5OH | CH2BrCH2Br |
A. A B. B C. C D. D
【答案】B
【解析】A项,Al与O2反应生成Al2O3,Al2O3与NaOH反应生成NaAlO2和H2O,NaAlO2溶液与过量CO2反应生成Al(OH)3和NaHCO3,Al(OH)3与NaOH反应生成NaAlO2和H2O,Al2O3不能一步生成Al(OH)3;B项,Fe3O4与CO高温反应生成Fe和CO2,Fe与HCl反应生成FeCl2和H2,Fe与Cl2加热时反应生成FeCl3,FeCl2与Cl2反应生成FeCl3,FeCl3与Fe反应生成FeCl2;C项,Cu与浓H2SO4加热反应生成CuSO4、SO2和H2O,SO2与H2S反应生成S和H2O,SO2发生催化氧化反应生成SO3,S与SO3相互间不能一步转化;D项,CH3CH2Br在NaOH醇溶液中发生消去反应生成CH2=CH2,CH2=CH2与H2O一定条件下发生加成反应生成C2H5OH,CH2=CH2与Br2发生加成反应生成CH2BrCH2Br,C2H5OH与CH2BrCH2Br相互间不能一步转化。
A项,Al与O2反应生成Al2O3,Al2O3与NaOH反应生成NaAlO2和H2O,NaAlO2溶液与过量CO2反应生成Al(OH)3和NaHCO3,Al(OH)3与NaOH反应生成NaAlO2和H2O,Al2O3不能一步生成Al(OH)3,Y→W不能一步实现;B项,Fe3O4与CO高温反应生成Fe和CO2,Fe与HCl反应生成FeCl2和H2,Fe与Cl2加热时反应生成FeCl3,FeCl2与Cl2反应生成FeCl3,FeCl3与Fe反应生成FeCl2,图中反应均能一步实现;C项,Cu与浓H2SO4加热反应生成CuSO4、SO2和H2O,SO2与H2S反应生成S和H2O,SO2发生催化氧化反应生成SO3,S与SO3相互间不能一步转化,Z与W间的相互转化不能一步实现;D项,CH3CH2Br在NaOH醇溶液中发生消去反应生成CH2=CH2,CH2=CH2与H2O一定条件下发生加成反应生成C2H5OH,CH2=CH2与Br2发生加成反应生成CH2BrCH2Br,C2H5OH与CH2BrCH2Br相互间不能一步转化,Z与W间的相互转化不能一步实现;答案选B。


科目:高中化学 来源: 题型:
【题目】以CO2和H2为原料制取乙醇的反应为 2CO2(g)+6H2(g)CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下 的密闭容器中,按CO2和H2的物质的量比为 1∶3 投料,不同温度下,达到平衡后平衡体系中各物质的物质的量分数(y%)随温度变化如图所示。下列说法正确的是
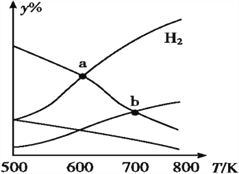
A. a点的平衡常数小于b点 B. b点:v正(CO2)=v逆(H2O)
C. a点:n(H2)=n(H2O) D. 温度不变,充入更多H2,v(CO2)始终不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:Ti(s) +2Cl2(g) = TiCl4(l) △H = -804.2 kJ ·mol-1;
2Na(s) +Cl2(g) = 2NaCl(s) △H = -882.0 kJ ·mol-1
Na(s) = Na(l) △H =2.6 kJ ·mol-1
请写出用液态钠与四氯化钛置换出钛的热化学方程式__________________________。
(2)已知:向一个体积恒定为2L的密闭容器中充入4mol A、1mol B,发生如下反应:4A(g)+B(s) ![]() 3C(s)+4D(g)。该反应中各物质的摩尔质量(单位g·mol-1)都不一样,在一定条件下该反应2分钟达到平衡。
3C(s)+4D(g)。该反应中各物质的摩尔质量(单位g·mol-1)都不一样,在一定条件下该反应2分钟达到平衡。
①不能够说明该反应已达到平衡的是:________。
A.恒温下,容器内的压强不再变化
B.恒温下,容器内混合气体的密度不再变化
C.一定条件下,D的体积分数保持不变
D.一定条件下,单位时间内消耗4molA的同时生成1 mol B
②平衡后测得D的浓度为0.3mol·L-1,则从反应开始到平衡时,A的平均反应速率为________,B转化率为________。
(3)用活性炭还原法可以处理氮氧化物,有关反应为:2NO(g)+C(s) ![]() N2(g)+CO2(g);△H,向某密闭容器加入一定量的活性炭和NO,在t℃下反应,有关数据如图:
N2(g)+CO2(g);△H,向某密闭容器加入一定量的活性炭和NO,在t℃下反应,有关数据如图:
NO | N2 | CO2 | |
起始浓度/molL─1 | 0.10 | 0 | 0 |
平衡浓度/molL─1 | 0.04 | 0.03 | 0.03 |
①在t℃下,该反应的平衡常数为________(保留两位有效数字)。
②平衡后升高温度,再次达到平衡,测得容器中NO、N2、CO2的浓度之比为2:1:1,则该反应的
ΔH________0(填“>”、“<”或“=”),此时NO的转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验室需要配制500mL0.10mol/LNa2CO3溶液。
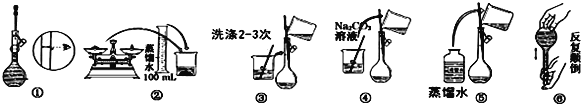
(1)所需玻璃仪器有:玻璃棒、烧杯、量筒、______、______。
(2)实验时图中所示操作的先后顺序为______(填编号)。
(3)在配制过程中,下列操作对所配溶液浓度如何?(填“偏高”、“偏低”或“无影响”)
①转移溶液后没有洗涤烧杯和玻璃棒______;
②向容量瓶加水定容时俯视液面______;
③摇匀后液面下降,再加水至刻度线______。
(4)所需Na2CO3固体的质量为__g;若改用浓溶液稀释,需要量取2mol/LNa2CO3溶液__mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学实验”已走近课堂,下列做法符合“绿色化学”理念的是

①实验室收集氨气采用图甲所示装置
②实验室中做氯气与钠反应的实验时采用图乙所示装置
③实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与HCl反应生成铵盐的实验
④实验室中采用图丙所示装置进行铜与稀硝酸的反应
A. ②③④ B. ①②③
C. ①②④ D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校研究性学习小组,探究一定量的浓硫酸与足量锌充分反应产生的气体产物,进行如下实验:按图组装好实验装置,在A中加入5 mL 98%的浓硫酸和足量的锌粒,微热试管A,观察到C、D、E中均有气泡产生;随后气泡量减少,品红溶液褪色,D中先出现浑浊后浑浊消失;反应较长时间后,C、D、E中的气泡量又会明显增加。
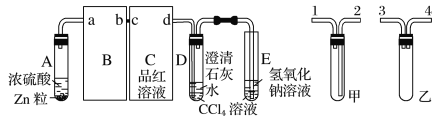
试回答下列问题:
(1)写出A中从反应开始到停止可能发生反应的化学方程式:_________________________________________。
(2)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接____、____接b,c接____、____接d;D、E两支试管中CCl4的作用是_______________________________。
(3)能证明浓硫酸具有强氧化性的实验现象为___________________________________;反应较长时间后气泡量又会明显增加的原因是_________________________________。
(4)D中浑浊消失的离子反应方程式为_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图所示装置进行实验,将液体A逐滴加入到固体B中,下列叙述不正确的是
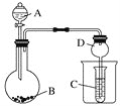
A. 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解
B. 若A为醋酸,B为贝壳,C中盛Na2SiO3,则C中溶液中变浑浊
C. 若A为浓盐酸,B为KMnO4,C中盛品红溶液,则C中溶液褪色
D. 实验仪器D可以起到防止溶液倒吸的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
A. 一定条件下,将1g乙炔溶于12g苯,所得混合物中含有的碳原子数为NA
B. l04g苯乙烯(C6H5-CH=CH2)中含有8NA个碳氢键和NA个碳碳双键
C. 在100g质量分数为46%的乙醇水溶液中,含有氢原子数为6NA
D. lmol有机物CH3-CH=CH-CH3中最多有8NA个原子在同一平面上
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com