
元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。请用相关的化学术语回答下列问题:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA[ | 0 |
2 |
|
|
| ⑤ |
| ⑥ | ⑦ |
|
3 | ① | ③ | ④ |
|
|
| ⑧ | ⑨ |
4 | ② |
|
|
|
|
|
|
|
(1) 在这些元素中,最不活泼的是 ,非金属性最强的是___________,金属性最强的是___________;(填元素符号或化学式,下同。)
(2) 这些元素形成的最高价氧化物对应的水化物中碱性最强的 ,酸性最强的__________;
(3) ①、②、③、④、⑤这五种元素的原子半径由大到小的顺序为 ;
(4) ⑥的氢化物的电子式为 ,① 在空气中燃烧后生成产物的电子式 。
科目:高中化学 来源:2017届湖南省、永兴一中高三上学期8月月考化学试卷(解析版) 题型:选择题
下列物质既能与盐酸反应,又能与氢氧化钠溶液反应的是
①Ba(OH)2 ②Al ③NaHCO3 ④Al2O3 ⑤NaHSO4 ⑥氨基酸 ⑦NH4HS
A.②④⑥ B.②③⑤⑥ C.①③④⑥ D.②③④⑥⑦
查看答案和解析>>
科目:高中化学 来源:2017届湖北省枣阳市高三上学期8月月考化学试卷(解析版) 题型:选择题
下列各组有机物中,只需加入溴水就能鉴别的是( )
A.已烯、苯、四氯化碳 B.苯、已炔、已烯
C.已烷、苯、环已烷 D.甲苯、已烷、已烯
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上8月月考化学试卷(解析版) 题型:实验题
FeCl3在现代工业生产中应用广泛。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。工业上,向500—600℃的铁屑中通入氯气可 生产无水氯化铁;向炽热铁屑中通入氯化氢可以生产无水氯化亚铁。
生产无水氯化铁;向炽热铁屑中通入氯化氢可以生产无水氯化亚铁。
某化学研究性学习小组模拟工业生产流程制备无水FeCl3并对产物做了如下探究实验,

请回答下列问题:
(1)装置的连接顺序为 (用a、b、c…h表示)。
(2)i.E中饱和食盐水的作用是 。
ii.D中碱石灰的作用是 。
(3)反应结束后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管B中硬质玻璃管的右端。要使沉积得FeCl3进入收集器,需进行的操作是 。
(4)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

①淡黄色溶液中加入试剂X生成淡红色溶液的离子方程式为
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是 (用离子方程式表示)。
(5)已知红色褪去的同时有气体生成,经检验为O2。该小组同学对红色褪去的原因进行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
②另取同物质的量浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
实验①说明 ;
实验②的目的是 ;
得出结论: 。
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上8月月考化学试卷(解析版) 题型:选择题
下列物质能用化合反应直接制得的是( )
①FeCl2 ②Fe(OH)3 ③NaHCO3 ④Fe(OH)2
A.② B.②③ C.①②③ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2016-2017年新疆兵团第二师华山中学高二上学前考化学卷(解析版) 题型:选择题
下列事实不能作为实验判断依据的是
A.钠和镁分别与冷水反应,判断金属活动性强弱
B.在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属活动性强弱
C.硫酸与碳酸的酸性比较,判断硫与碳的非金属活动性强弱
D.1moLBr2和1moLI2分别与足量的H2反应,判断溴与碘的非金属性强弱
查看答案和解析>>
科目:高中化学 来源:2016-2017年新疆兵团第二师华山中学高二上学前考化学卷(解析版) 题型:选择题
200℃,11.6g二氧化碳和水的混合气体与足量的过氧化钠反应,反应后固体质量增加了3.6g。则原气态混合物的平均相对分子质量为
A.5.8 B.11.6 C.23.2 D.46.4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上入学考化学试卷(解析版) 题型:选择题
下列除去杂质的方法中,错误的是
选项 | 物质 | 杂质 | 除杂质的方法 |
A. | 稀硫酸 | 铜 | 过滤 |
B. | CaSO4溶液 | 稀硫酸 | 过量CaCO3、过滤 |
C. | FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
D. | 二氧化碳 | 一氧化碳 | 点燃 |
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第一次月考化学试卷(解析版) 题型:填空题
短周期元素a、b、c、d的原子序数依次增大,c和d位于同主族且原子序数相差8;基态a原子核外有3个能级上容纳电子且每个能级上电子数相等,c原子s能级电子总数与p能级电子数相等,基态e原子的M层上有2个未成对电子且无空轨道。
(1)在a、b、c中,第一电离能由大到小排序为 (用元素符号表示);基态e原子的价层电子排布式为 。
(2)配合物e(ac)4在常温下呈液态,易溶于四氯化碳、苯等有机溶剂。固态e(ac)4的晶体类型是 。已知(dab)2分子中含非极性键,分子中每个原子最外层都达到8个电子稳定结构,1mol(dab)2分子含σ键的数目为 。
(3)写出一种与dab-互为等电子体的分子 (填化学式)。ac32-的中心原子杂化类型为 ;dc32-的空间构型为 。
(4)ec晶胞结构如图所示,其晶胞参数为a pm,列式计算该晶胞的密度为 g·cm-3(不必计算出结果,阿伏伽德罗常数的值为NA),晶胞中c粒子的配位数为 。
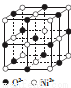
(5)人工合成的ec晶胞存在缺陷,即阳离子有+3、+2价两种。某人工合成的晶体样品组成为e0.96c,则该晶体中+3价、+2价两种离子的个数之比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com