
工业上利用CO和水蒸气在一定条件下发生反应制取氢气:CO(g)+H2O(g)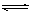 CO2(g)+H2(g)某研究小组分别在体积均为2L的恒容密闭容器中加入一定量的反应物,使其发生反应,相关数据如下:
CO2(g)+H2(g)某研究小组分别在体积均为2L的恒容密闭容器中加入一定量的反应物,使其发生反应,相关数据如下:
|
容器编号 |
温度℃ |
起始量/mol |
平衡量/mol |
达到平衡的时间/min |
达到平衡时体系能量的变化/kJ |
||
|
CO |
H2O |
CO2 |
H2 |
||||
|
① |
650 |
1 |
2 |
0.4 |
0.4 |
5 |
16.4 |
|
② |
650 |
2 |
4 |
|
|
t1 |
Q1 |
|
③ |
900 |
2 |
4 |
1.6 |
1.6 |
t2 |
Q2 |
(1)计算容器②中反应的平衡常数K=_____________(计算结果保留两位小数)。
(2)容器③中反应达平衡时,CO的转化率为____________。
(3)容器①中反应达平衡这段时间,化学反应速率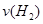 =__________。
=__________。
(4)该反应的正反应为_______(填“吸热”或“放热”)反应,理由是____________。
(5)下列叙述正确的是____________(填字母序号)。
a.平衡时,容器①和容器②中CO2的体积分数相等
b.反应达平衡状态时,Q2>Q1>32.8kJ
c.达到平衡的时间:t2>t1>2.5min
d.该反应的热化学方程式可表示为:CO(g)+H2O(g)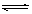 CO2(g)+H2(g) △H=
-41kJ/mol
CO2(g)+H2(g) △H=
-41kJ/mol
(1)0.17(2)80℅(3)0.04mol/L(4)吸热 升高温度,反应物的转化率增大。(5)a
【解析】
试题分析:(1)化学平衡常数只跟反应温度有关,而与投料方式无关,对于①②化学平衡常数一样。K={C(CO2)·C(H2)}∕{C(CO)·C(H2O)}=(0.2×0.2) ∕{(0. 5-0.2) ×(1-0.2)}=1∕6=0.17.(2)对于容器③达到化学平衡时二氧化碳、氢气的平衡浓度为0.8mol∕L,则消耗的CO、 H2O的浓度也是0.8mol∕L。所以C(CO)(平衡)=(1-0.8)mol∕L=0.2 mol∕L;C(H2O)(平衡)=(2-0.8)mol∕L=1.2 mol∕L。 CO的转化率为:(0.8∕1)×100℅=80℅。(3)容器①中反应达平衡这段时间,化学反应速率V(H2)=ΔC(H2) ∕Δt={(0.4-0) mol∕2L}∕5min=0.04
mol∕(L·min) (4) 容器②假设CO转化浓度为X,K={C(CO2)·C(H2)}∕{C(CO)·C(H2O)}=X2
∕{(1-X) ×(2-X)} =1∕6.解得X=0.4 mol∕L.所以CO转化率为:(0.4∕1)×100℅=40℅。容器②③只是温度不同,起始投料相同,但CO的转化率前者是40℅,后者是80℅。可见反应物的转化率增大。根据勒夏特列原理可知升高温度化学平衡向吸热方向移动。故正反应是吸热反应。(5) a.容器①和容器②中投料比例相同,反应又是在相同温度下进行,所以反应物的转化率相同,产物的含量即体积分数相同,正确。b.该反应是气体体积相等的可逆反应。改变压强平衡不移动。由于容器②的物质的量是①的2倍,所以能量转化也是①的2倍。即Q1=32.8kJ。容器③与②比较:③温度高升。升高温度化学平衡向正反应方向移动。转化时能量变化比②多。达平衡状态时,Q2>Q1
所以反应达平衡状态时,Q2>Q1=32.8kJ。错误。c.在其它条件不变的情况下,增大反应物的浓度,化学反应速率越快;升高温度,化学反应速率越快,达到平衡所需时间就越短。所以达到平衡的时间:t2<t1<2.5min。错误。d.该反应的正反应是吸热反应。所以其热化学方程式应表示为:CO(g)+H2O(g)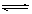 CO2(g)+H2(g) △H=
+41kJ/mol。错误。
CO2(g)+H2(g) △H=
+41kJ/mol。错误。
考点:考查可逆反应的化学平衡常数、反应物的转化率、反应速率等问题的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 容器 编号 |
温度 /℃ |
起始量/mol | 平衡量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||
| CO | H2O | CO2 | H2 | ||||
| ① | 650 | 1 | 2 | 0.4 | 0.4 | 5 | 16.4kJ |
| ② | 650 | 2 | 4 | t1 | Q1 kJ | ||
| ③ | 900 | 2 | 4 | 1.6 | 1.6 | t2 | Q2 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常数 | 64.0 | 50.7 | 42.9 |
| c3(CO3) |
| c3(CO) |
| c3(CO3) |
| c3(CO) |
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8kJ | |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q | |
| 4 |
| Vt1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ | |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q | |
| 4 |
| Vt1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ | |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q | |
| 4 |
| Vt1 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ | |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q | |
| 4 |
| Vt1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com