
为配制0.1mol/L的NaOH溶液,下列说法中正确的是()
A. 取4g NaOH固体溶于1L水中
B. 取0.4g NaOH固体溶于水配成1L溶液
C. 取4g NaOH固体溶于水配成1L溶液
D. 取0.4g NaOH固体溶于1L水中
考点: 配制一定物质的量浓度的溶液.
专题: 物质的量浓度和溶解度专题.
分析: 0.1mol/L的NaOH溶液的意义是:1L溶液中含有氢氧化钠的物质的量为0.1mol,注意1L是指溶液的体积,不是溶剂的体积.
解答: A.取4g NaOH固体溶于1L水中,4g NaOH的物质的量为=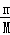 =
=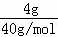 =0.1mol,溶剂的体积为1L,溶液的物质的量浓度小于0.1mol/L,故A错误;
=0.1mol,溶剂的体积为1L,溶液的物质的量浓度小于0.1mol/L,故A错误;
B.0.4g NaOH的物质的量为=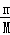 =
=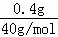 =0.01mol,溶液的体积为1L,所以溶液的物质的量浓度为
=0.01mol,溶液的体积为1L,所以溶液的物质的量浓度为 =
=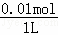 =0.01mol/L,故B错误;
=0.01mol/L,故B错误;
C.4g NaOH的物质的量为=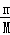 =
=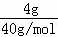 =0.1mol,溶液的体积为1L,溶液的物质的量浓度等于0.1mol/L,故C正确;
=0.1mol,溶液的体积为1L,溶液的物质的量浓度等于0.1mol/L,故C正确;
D.0.4g NaOH的物质的量为= =
=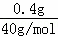 =0.01mol,溶剂的体积为1L,溶液的物质的量浓度小于0.01mol/L,故D错误;
=0.01mol,溶剂的体积为1L,溶液的物质的量浓度小于0.01mol/L,故D错误;
故选:C.
点评: 本题考查氢氧化钠溶液的配制,题目难度不大,本题注意溶剂的体积不等于溶液的体积,注意二者的区别是解题关键.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
已知:R﹣OH+R﹣OH R﹣O﹣R(醚)+H20,分子式为C2H6O和C3HsO醇的 混合物在一定条件下脱水形成的醚最多有( )
R﹣O﹣R(醚)+H20,分子式为C2H6O和C3HsO醇的 混合物在一定条件下脱水形成的醚最多有( )
|
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)电镀是将镀件与电源的 极连接。
(2)化学镀的原理是利用化学反应生成金属单质沉淀在镀件表面形成的镀层。
①若用铜盐进行化学镀铜,应选用 (填“氧化剂”或“还原剂”)与之反应。
②某化学镀铜的反应速率随镀液pH变化如右图所示。该镀铜过程中,镀液pH控制在12.5左右。据图中信息,给出使反应停止的方法: 。
(3)酸浸法制取硫酸铜的流程示意图如下:

①步骤(i)中Cu2(OH)2CO3发生反应的化学方程式为 。
②步骤(ii)所加试剂起调节pH作用的离子是 (填离子符号)。
③在步骤(iii)发生的反应中,1molMnO2转移2 mol电子,该反应的离子方程式为:
。
④步骤(iv)除去杂质的化学方程式可表示为
3Fe3++NH4++2SO42-+6H2O=NH4Fe3(SO4)2(OH)6↓+6H+,过滤后母液的pH=2.0,
c(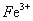 )=a mol·L—1,c(
)=a mol·L—1,c( )=b mol·L—1,c(
)=b mol·L—1,c(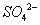 )=d mol·L—1,
)=d mol·L—1,
该反应的平衡常数K= (用含a、b、d的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
2011年3月日本地震引起福岛核电站事故后,引起很多恐慌,人们担心受到核污染.按照国际规定,凡是可能形成和污染的物品与场所,以及有危险的药品和试剂,都必须张贴各种警示标志,以提醒大家注意防护.下列标志中用于表示辐射标志的是()
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
下面关于电解质的叙述中错误的是()
A. 在水溶液中或熔融状态下均不导电的化合物叫非电解质
B. 电解质、非电解质都指化合物而言,单质不属于此范畴
C. 电解质在水中一定能导电,在水中导电的化合物一定是电解质
D. BaSO4不溶于水,但BaSO4是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列药品置于空气中很容易变质(括号内的物质是变质后的物质),其中是因为氧化还原反应而变质的是()
A. Ca(OH)2[CaCO3] B. Fe(OH)3[Fe2O3] C. KI[I2] D. NaOH[Na2CO3]
查看答案和解析>>
科目:高中化学 来源: 题型:
一包白色固体可能含有CuSO4、CaCO3、Na2CO3、NaCl中的一种或几种,为确定其成分取一定量的固体依次作如下实验
(1)溶于水得到无色溶液.
(2)向溶液中滴加过量的稀盐酸有气泡产生,该气体能使澄清的石灰水变浑浊.
(3)向(2)的溶液中滴加稀硝酸和硝酸银溶液有白色沉淀产生.则固体中
①一定含有的物质是 (填化学式);
②一定没有的物质是 (填化学式);
③不能确定是否含有的是 (填化学式),确定该物质是否含有的试验方法为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com