
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、SiO32-、Cl-、NO3- | B. | Cu2+、NH4+、Al3+、SO42- | ||
| C. | Na+、S2-、OH-、SO42- | D. | Na+、ClO-、CH3COO-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
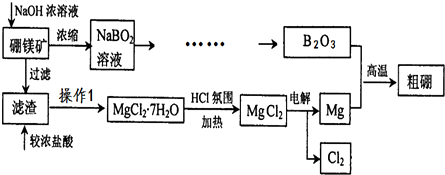

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知可逆反应:2SO2+O2?2SO3,当O2的消耗速率与SO3的消耗速率之比为1:2时,表明该可逆反应达到化学平衡状态 | |
| B. | 由Zn、Cu、稀硫酸组成的原电池,负极为Zn,发生还原反应,电极反应式为:Zn-2e-=Zn2+ | |
| C. | 工业上金属Mg、Al都是用电解熔融的氯化物制得的 | |
| D. | 甲苯的一氯代物有4种,则甲苯与足量H2发生加成反应后所得到的有机产物的一氯代物也只有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 步骤和现象 | 现象 |
| Ⅰ.将等体积等浓度的AgNO3溶液和NaCl溶液混合得到浊液W,过滤,得到滤液X和白色沉淀Y | |
| Ⅱ.向滤液X中滴加几滴饱和Na2S溶液 | 出现浑浊 |
| Ⅲ.取少量白色沉淀Y,滴加几滴饱和Na2S溶液 | 沉淀变为黑色 |
| Ⅳ.取少量白色沉淀Y,滴加几滴浓氨水 | 沉淀逐渐溶解 |
 Ag+(aq)+Cl-(aq).
Ag+(aq)+Cl-(aq). Ag+(aq)+Cl-(aq),银离子与氨水结合,降低了溶液中银离子的浓度,使上述平衡正向移动,促使AgCl溶解.
Ag+(aq)+Cl-(aq),银离子与氨水结合,降低了溶液中银离子的浓度,使上述平衡正向移动,促使AgCl溶解.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL 0.01mol/L的CH3COOH溶液与10mL 0.1mol/L的CH3COOH溶液的H+数目 | |
| B. | 常温下pH=4的KHSO4溶液和CH3COOK溶液中由水电离出的OH-离子浓度 | |
| C. | 纯水在100℃时的pH和25℃时的pH | |
| D. | 100mL 0.01mol/L的CH3COOH溶液与10mL 0.1mol/L的CH3COOH溶液的H+浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol苯乙烯能与4mol H2发生加成反应,说明其分子内含有4个碳碳双键 | |
| B. | 用浓Na2SO4、CuSO4溶液或浓硝酸溶液使蛋清液发生盐析,进而分离、提纯蛋白质 | |
| C. | 淀粉水解与纤维素水解时所生成的最终产物不相同 | |
| D. | 油脂可以与NaOH溶液发生皂化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com