
【题目】实验室用乙醇和浓硫酸加热制取乙烯,实验装置如图,制备过程中,常会看到烧瓶中液体变黑,并有刺激性气味气体(SO2)产生。
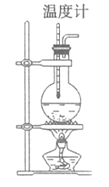
(1)制备乙烯的化学方程式_________。
(2)加热至140℃时发生副反应,写出该反应有机产物的结构简式__________,该反应的反应类型为:__________。
(3)写出产生SO2的化学方程式:___________。
(4)图中一处明显的错误是__________,加入碎瓷片的作用是__________。
(5)有人设计下列实验以确认上述混合气体中有乙烯和SO2。装置①、②、③、④可盛放的试剂是①__________;②__________;③品红;④__________。(填字母)

A. 品红溶液 B. NaOH溶液 C. 浓H2SO4 D. 酸性KMnO4溶液
(6)实验(5)中确认含有乙烯的现象是____________________。
【答案】CH3CH2OH![]() CH2=CH2↑+H2O CH3CH2OCH2CH3 取代反应 C+2H2SO4(浓)
CH2=CH2↑+H2O CH3CH2OCH2CH3 取代反应 C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O 温度计水银球未插入到液面以下 防止暴沸 A B D 装置③中的品红溶液不褪色,装置④中的KMnO4酸性溶液褪色
CO2↑+2SO2↑+2H2O 温度计水银球未插入到液面以下 防止暴沸 A B D 装置③中的品红溶液不褪色,装置④中的KMnO4酸性溶液褪色
【解析】
(1)乙醇和浓硫酸混合加热,温度迅速上升到170°C即可制备乙烯,据此书写化学方程式;
(2)加热至140℃时发生副反应,生成乙醚和水,该反应的反应类型为取代反应;
(3)碳和浓硫酸共热产生SO2;
(4)图中一处明显的错误是温度计的位置出错了,加入碎瓷片的作用是防暴沸;
(5)从实验目的确定试剂和连接顺序;
(6)实验(5)中确认含有乙烯的现象是已排查干扰气体存在的前提下,可检验乙烯的高锰酸钾溶液褪色了,现象要写全。
(1)乙醇和浓硫酸混合加热,温度迅速上升到170°C即可制备乙烯,则化学方程式为CH3CH2OH![]() CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
答案为:CH3CH2OH![]() CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
(2)加热至140℃时发生副反应,生成乙醚和水,该反应的化学方程式为2CH3CH2OH![]() CH3CH2OCH2CH3+H2O,有机产物的结构简式为CH3CH2OCH2CH3,该反应类型为取代反应;
CH3CH2OCH2CH3+H2O,有机产物的结构简式为CH3CH2OCH2CH3,该反应类型为取代反应;
答案为:CH3CH2OCH2CH3;取代反应;
(3)实验过程中液体发黑,因为乙醇部分转变为碳,则碳和浓硫酸共热时发生氧化还原反应,产生SO2,化学方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;
CO2↑+2SO2↑+2H2O;
答案为:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;
CO2↑+2SO2↑+2H2O;
(4)温度计的作用是测液体反应液的温度,所以温度计要插入到液面下,加入碎瓷片的作用是防暴沸;
答案为:温度计水银球未插入到液面以下;防止暴沸;
(5) 要确认上述混合气体中有乙烯和SO2,装置连接的顺序应该是检验SO2、吸收SO2、检验SO2已除尽、检验乙烯,对应的溶液为品红溶液、NaOH溶液、品红溶液、高锰酸钾酸性溶液,则选择A;B;D;
答案为:A;B;D;
(6)实验(5)中确认含有乙烯的现象是已排查干扰气体存在的前提下,可检验乙烯的高锰酸钾或溴水褪色了,即装置③内品红溶液不褪色确认SO2已除干净,装置④高锰酸钾酸性溶液褪色检验乙烯;
答案为:装置③中的品红溶液不褪色,装置④中的KMnO4酸性溶液褪色。


科目:高中化学 来源: 题型:
【题目】如图是德国化学家李比希1831年测定烃类化合物(只含C、H两种元素)组成的装置。瓷舟内的烃样品经加热分解或气化后用纯![]() 流驱赶经过灼热的
流驱赶经过灼热的![]() ,这里烃类化合物反应变成
,这里烃类化合物反应变成![]() 和
和![]() ,经吸收管吸收。
,经吸收管吸收。

已知下表数据:
瓷舟 | 吸收管Ⅰ | 吸收管Ⅱ | |||
瓷舟 | 样品+瓷舟 | 吸收前 | 吸收后 | 吸收前 | 吸收后 |
A | B | C | D | E | F |
(1)烃样品在反应过程中所用的氧化剂是________________________;
(2)吸收管Ⅰ应装的吸收剂是____________,吸收管Ⅱ应装的吸收剂是____________;
(3)样品中碳的质量分数的数学表达式是________________________;
(4)取该烃![]() 在氧气中充分燃烧后,生成
在氧气中充分燃烧后,生成![]() 和
和![]() 。若该烃在一定条件下能与氯气发生取代反应,且其一氯代物只有一种,则烃A的结构简式为___________,用系统命名法命名为____________。
。若该烃在一定条件下能与氯气发生取代反应,且其一氯代物只有一种,则烃A的结构简式为___________,用系统命名法命名为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铬具有极高的硬度和力学强度、优异的抗腐蚀性能和高温稳定性能,因而具有广泛应用前景。实验室制备CrN 反应原理为 CrCl3 +NH3![]() CrN+3HCl,装置如图所示
CrN+3HCl,装置如图所示
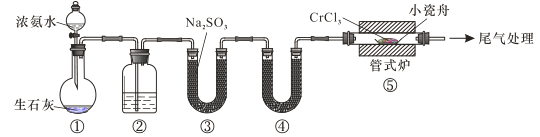
下列说法错误的是
A.装置①还可以用于制取O2、Cl2、CO2等气体
B.装置②、④中分别盛装NaOH溶液、KOH固体
C.装置③中也可盛装维生素c,其作用是除去氧气
D.装置⑤ 中产生的尾气冷却后用水吸收得到纯盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现艾滋病治疗药物利托那韦对新型冠状病毒也有很好的抑制作用,它的合成中间体2-异丙基-4-(甲基氨基甲基)噻唑可按如下路线合成:

回答下列问题:
(1)A的结构简式是__________,C中官能团的名称为 ______________。
(2)①、⑥的反应类型分别是__________、_____。D的化学名称是______。
(3)E极易水解生成两种酸,写出E与NaOH溶液反应的化学方程式:_______。
(4)H的分子式为 __________________。
(5)I是相对分子质量比有机物 D 大 14 的同系物, 写出I 符合下列条件的所有同分异构体的结构简式:_____________。
①能发生银镜反应 ②与NaOH反应生成两种有机物
(6)设计由 ,和丙烯制备
,和丙烯制备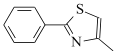 的合成路线______________(无机试剂任选)。
的合成路线______________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子液体是一种由离子组成的液体,在低温下也能以液态存在,是一种很有研究价值的溶剂。研究显示最常见的离子液体主要由图示正离子和负离子组成:

回答下列问题:
(1)按电子排布,Al划分在元素周期表中的______区(填“s”“p”“d”或“ds”),图中负离子的空间构型为____________________。
(2)基态Cl原子的价电子排布图为____________________。
(3)图中正离子有令人惊奇的稳定性, 它的电子在其环外结构中高度离域。该正离子中C原子的杂化方式为_________。该化合物中不存在____(填标号)。
A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键
(4)C、N、H三种元素的电负性由大到小的顺序为 __________,NH3与CH4的中心原子均为 sp3杂化,但是H-N-H 的键角小于H-C-H的键角,原因是________。
(5)AlN是一种陶瓷绝缘体,具有较高的导热性和硬度, 其立方晶胞如图所示,Al原子周围紧邻的Al原子有_____个。已知:氮化铝的密度为dg/cm3, 阿伏加德罗常数为NA,则最近的N原子与Al原子间的距离为_____________pm。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜和硫的化合物在化工、医药材料等领域具有广泛的用途。回答下列问题:
(1)原子轨道是指电子在原子核外的___________,基态S原子的原子轨道数是____个。
(2)基态Cu原子中,核外电子占据的原子轨道为球形的最高能级符号是______,占据该能级的电子数为__________。
(3)Cl、S、Se在元素周期表中处于相邻的位置,其第一电离能的大小顺序为_______。
(4)下图是含元素Cu、S的有机物的结构简式:

①该有机化合物结构中含有的化学键类型是_______(填“共价键““离子键”或“共价键、离子键”)、配位键,其中1个该有机物分子中配位键数为_____个,这些配位键中提供孤电子对的元素是__________。
②S原子的杂化方式为_______、带*N原子的杂化方式为_______。
(5)下图是Cu-Au合金的一种立方晶体结构:

已知该合金的密度分dg/cm3,阿伏加德罗常数的值为NA,若Au原子的半径为bpm(lpm=10-10cm),则铜原子的半径为______cm(写出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是同周期主族元素,Y 的最外层电子数是 X 次外层电子数的 3倍,四种元素与锂组成的盐是一种新型电池的电解质(结构如图,箭头指向表示共用电子对由 W 提供)。下列说法不正确的是( )
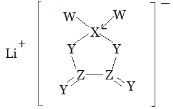
A.W的非金属性比Y的强
B.原子半径Z比X大
C.该物质中含离子键和共价键
D.该物质中Ⅹ原子满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子结构与元素周期表存在着内在联系。根据所学物质结构知识,请回答下 列问题:
(1)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严 重危害人们健康。苏丹红常见有Ⅰ、Ⅱ、Ⅲ、Ⅳ4 种类型,苏丹红Ⅰ的分子结构如图所示:
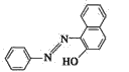
苏丹红Ⅰ在水中的溶解度很小,微溶于乙醇,有人把羟基取代在对位形成如图所示的结构:
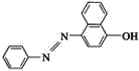
则其在水中的溶解度会_____(填“增大”或“减小”),原因是_____。
(2)已知 Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一种为绿色。两种晶体的组成皆为 TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:a.分别取等质量的两种配合物晶体的样品配成待测溶液;b.分别往待测溶液中滴入 AgNO3 溶液,均产生白色沉淀;c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液得到的白色沉淀质量为原紫色晶体的水溶液得到的沉淀质量的2/3。则绿色晶体配合物的化学式为_______,由 Cl-所形成的化学键类型是_______。
(3)如图中A、B、C、D四条曲线分别表示第ⅣA、ⅤA、ⅥA、ⅦA族元素的氢化物的沸点,其中表示ⅦA族元素氢化物沸点的曲线是_____;表示ⅣA族元素氢化物沸点的曲线是_____;同一族中第3、4、5周期元素的氢化物沸点依次升高,其原因是__________;A、B、C曲线中第二周期元素的氢化物的沸点显著高于第三周期元素的氢化物的沸点,其原因是_______________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com