
| A£® | F2£¾Cl2£¾Br2£¾I2 | B£® | CF4£¾CCl4£¾CBr4£¾CI4 | ||
| C£® | HF£¼HCl£¼HBr£¼HI | D£® | CH4£¼SiH4£¼GeH4£¼SnH4 |
·ÖĪö A£®Ā±×åŌŖĖŲÖŠ£¬Ō×ÓŠņŹżŌ½“󣬵„ÖŹµÄČŪ·ŠµćŌ½øߣ»
B£®ĖÄÖÖĪļÖŹµÄĻą¶Ō·Ö×ÓĮæŌ½“󣬷Ö×Ó¼ä×÷ÓĆĮ¦Ō½Ē棬ČŪ·ŠµćŌ½øߣ»
C£®·ś»ÆĒāÖŠ“ęŌŚĒā¼ü£¬Ōņ·ś»ÆĒāµÄ·Šµć×īøߣ»
D£®ĖÄÖÖĒā»ÆĪļµÄĻą¶Ō·Ö×ÓÖŹĮæŌ½“ó£¬Ęä·ŠµćŌ½øߣ®
½ā“š ½ā£ŗA£®Ā±ĖŲµ„ÖŹÖŠ£¬Ō×ÓŠņŹżŌ½“󣬶ŌÓ¦µ„ÖŹµÄČŪ·ŠµćŌ½“ó£¬ŌņČŪ·Šµć“óŠ”ĪŖ£ŗF2£¼Cl2£¼Br2£¼I2£¬¹ŹA“ķĪó£»
B£®CF4”¢CCl4”¢CBr4”¢CI4µÄ¾§Ģ嶼ŹĒ·Ö×Ó¾§Ģ壬ČŪ·Šµć“óŠ”Óė·Ö×Ó¼ä×÷ÓĆĮ¦“óŠ”ÓŠ¹Ų£¬ŌņĖÄÖÖĪļÖŹµÄČŪ·ŠµćøßµĶĪŖ£ŗCF4£¼CCl4£¼CBr4£¼CI4£¬¹ŹB“ķĪó£»
C£®HF·Ö×ÓÖŠ“ęŌŚĒā¼ü£¬µ¼ÖĀĶ¬Ņ»Ö÷×åµÄĒā»ÆĪļÖŠHFµÄ·Šµć×īøߣ¬ŌņÕżČ·µÄ·ŠµćøßµĶĪŖ£ŗHCl£¼HBr£¼HI£¼HF£¬¹ŹC“ķĪó£»
D£®CH4”¢SiH4”¢GeH4”¢SnH4µÄ¾§Ģ嶼ŹĒ·Ö×Ó¾§Ģ壬Ļą¶Ō·Ö×ÓÖŹĮæŌ½“ó£¬Ēā»ÆĪļµÄČŪ·ŠµćŌ½øߣ¬ŌņČŪ·ŠµćøßµĶĪŖ£ŗCH4£¼SiH4£¼GeH4£¼SnH4£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖŌ×Ó½į¹¹ÓėŠŌÖŹ£¬ĢāÄæÄŃ¶Č²»“ó£¬Ć÷Č·Ó°ĻģĪļÖŹČŪ·ŠµćµÄÓ°ĻģĪŖ½ā“š¹Ų¼ü£¬CĪŖŅדķµć£¬×¢ŅāĒā¼ü“ęŌŚĒéæö¼°¶ŌĪļÖŹČŪ·ŠµćµÄÓ°Ļģ£¬ŹŌĢāÅąŃųĮĖѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
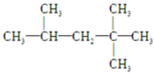 £¬ĖüŹĒĘūÓĶČ¼ÉÕĘ·ÖŹæ¹ÕšŠŌÄܵIJĪÕÕĪļ£¬ĘäÖŠAµÄĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬µČŠ§ĒāŌ×ÓÖÖĄą×īÉŁµÄŅ»ÖÖ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬ĖüŹĒĘūÓĶČ¼ÉÕĘ·ÖŹæ¹ÕšŠŌÄܵIJĪÕÕĪļ£¬ĘäÖŠAµÄĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬µČŠ§ĒāŌ×ÓÖÖĄą×īÉŁµÄŅ»ÖÖ½į¹¹¼ņŹ½ĪŖ£ŗ £»ČōAŹĒÓÉĻ©ĢžŗĶH2Ķعż¼Ó³É·“Ó¦µĆµ½£¬ŌņøĆĻ©ĢžµÄ½į¹¹¼ņŹ½ĪŖ
£»ČōAŹĒÓÉĻ©ĢžŗĶH2Ķعż¼Ó³É·“Ó¦µĆµ½£¬ŌņøĆĻ©ĢžµÄ½į¹¹¼ņŹ½ĪŖ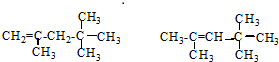 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĻĀĮŠøų³öĮĖĢž¼°ĢžµÄŃÜÉśĪļA”¢B”¢C”¢D”¢EµÄĻą¹ŲŠÅĻ¢£ŗ
ĻĀĮŠøų³öĮĖĢž¼°ĢžµÄŃÜÉśĪļA”¢B”¢C”¢D”¢EµÄĻą¹ŲŠÅĻ¢£ŗ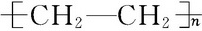 £®
£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
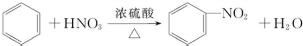
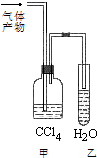 A”¢B”¢C”¢D”¢E”¢F ĮłÖÖÓŠ»śĪļ£®AÄܹ»ŌŚ¹āÕÕĢõ¼žĻĀÓėĀČĘų·¢ÉśČ”“ś·“Ó¦£¬Ę䶞ĀČČ”“śĪļÓŠĮ½ÖÖ£» BÓėäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗæÉŅŌ·¢Éś¼Ó³É·“Ó¦£¬¼Ó³É²śĪļŹĒD£¬ĒŅDÖ»ÓŠŅ»ÖÖĶ¬·ÖŅģ¹¹ĢåE£»CŌŚFeBr3 µÄ×÷ÓĆĻĀ£¬æÉŅŌÓėŅŗäå·¢ÉśČ”“ś·“Ó¦£¬Č”“ś²śĪļŹĒF£¬Fƻӊŗ¬±½»·µÄĶ¬·ÖŅģ¹¹Ģ壮øł¾ŻŅŌÉĻŹĀŹµ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
A”¢B”¢C”¢D”¢E”¢F ĮłÖÖÓŠ»śĪļ£®AÄܹ»ŌŚ¹āÕÕĢõ¼žĻĀÓėĀČĘų·¢ÉśČ”“ś·“Ó¦£¬Ę䶞ĀČČ”“śĪļÓŠĮ½ÖÖ£» BÓėäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗæÉŅŌ·¢Éś¼Ó³É·“Ó¦£¬¼Ó³É²śĪļŹĒD£¬ĒŅDÖ»ÓŠŅ»ÖÖĶ¬·ÖŅģ¹¹ĢåE£»CŌŚFeBr3 µÄ×÷ÓĆĻĀ£¬æÉŅŌÓėŅŗäå·¢ÉśČ”“ś·“Ó¦£¬Č”“ś²śĪļŹĒF£¬Fƻӊŗ¬±½»·µÄĶ¬·ÖŅģ¹¹Ģ壮øł¾ŻŅŌÉĻŹĀŹµ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com