
【题目】下列有关晶体的叙述中,不正确的是( )
A.金刚石的网状结构中,由共价键形成的碳原子环,其中最小的环上有6个碳原子
B.在氯化钠晶体中,每个Na+或Cl﹣的周围紧邻6个Cl﹣或6个Na+
C.干冰晶体熔化时,1mol干冰要断裂2mol碳氧双键
D.在氯化铯晶体中,每个Cs+周围紧邻8个Cl﹣ , 每个Cl﹣周围也紧邻8个Cs+
【答案】C
【解析】解:A.金刚石结构中,每个碳原子能形成4个共价键,由共价键形成的最小碳环上有6个碳原子,故A正确;
B、氯化钠的晶胞图为  ,则氯化钠晶胞中,钠离子的配位数为6,即每个Na+或Cl﹣的周围都紧邻6个Cl﹣或Na+ , 故B正确;
,则氯化钠晶胞中,钠离子的配位数为6,即每个Na+或Cl﹣的周围都紧邻6个Cl﹣或Na+ , 故B正确;
C.干冰晶体熔化时,碳氧双键不发生断裂,故C错误;
D.氯化铯的晶胞图为  ,在CsCl晶体中每个Cs+周围都紧邻8个Cl﹣ , 每个Cl﹣周围也紧邻8个Cs+ , 故D正确;
,在CsCl晶体中每个Cs+周围都紧邻8个Cl﹣ , 每个Cl﹣周围也紧邻8个Cs+ , 故D正确;
故选C.
【考点精析】本题主要考查了离子晶体和原子晶体的相关知识点,需要掌握离子间通过离子键结合而成的晶体叫作离子晶体;相邻原子间以共价键相结合而形成空间网状结构的晶体叫原子晶体才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】A,B,C,D 4种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1)B元素的名称为;
(2)A,B形成的化合物的电子式为 .
(3)C的元素符号为 , C的最高价氧化物的化学式为 .
(4)D的最高价氧化物对应的水化物的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是粒子直径为1nm~100nm (1nm=10-9m) 的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过半透膜 ⑥静置后,会析出黑色沉淀。其中正确的是
A. ①④⑥ B. ②③④ C. ②③⑤ D. ②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,主要以![]() 形式存在。化学课外小组将海带灼烧成灰,用水浸泡一段时间,得到海带灰悬浊液,然后按以下实验流程提取
形式存在。化学课外小组将海带灼烧成灰,用水浸泡一段时间,得到海带灰悬浊液,然后按以下实验流程提取![]() 单质(已知
单质(已知![]() 可以氧化
可以氧化![]() ):
):
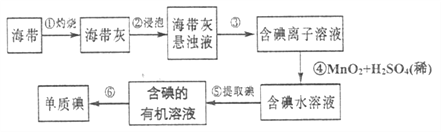
(1)指出制取碘的过程中有关的实验操作名称:③_________⑤__________。
(2)提取碘的过程中,可供选择的有机溶剂是__________(填字母代号)。
A. 酒精 B. ![]() C. 醋酸
C. 醋酸
(3)步骤④中每消耗![]() 转移
转移![]() 电子,生成
电子,生成![]() ,则发生反应的离子方程式为___________。
,则发生反应的离子方程式为___________。
(4)为实现步骤⑤的转化,实验室里有烧杯、玻璃棒、量简以及必要的夹持仪器、物品。尚缺少的玻璃仪器是___________。
(5)多次通过步骤⑤操作,可获取较高浓度的含碘有机溶液。若从中再提取![]() ,可以加入
,可以加入![]() 的
的![]() 溶液,将
溶液,将![]() 转化成可溶于水的含碘化合物:
转化成可溶于水的含碘化合物: ![]() 。经操作I分离得到含碘化合物的水溶液,再向其中加入过量的45%的硫酸溶液,生成
。经操作I分离得到含碘化合物的水溶液,再向其中加入过量的45%的硫酸溶液,生成![]() 沉淀,经操作II获得碘单质。则操作I的名称是_________,操作II的名称是________(填字母)。
沉淀,经操作II获得碘单质。则操作I的名称是_________,操作II的名称是________(填字母)。
A. 过滤 B. 蒸发 C. 蒸馏 D. 分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学课上,围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。请回答:
(1)生成的黑色(单质)物质是__________ (填化学式)。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是___________ (填化学式),这种黑色物质继续与浓硫酸作用,产生两种气体的化学方程式为:______________________________________。
(3)据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有__________(填序号)。
A.酸性 B.吸水性 C.脱水性 D.强氧化性
(4)将实验(2)产生的刺激性气味气体通入品红溶液,可以看到品红溶液_________ 说明这种气体具有_____________________性;将(2)中产生的刺激性气味的气体通入水中可生成一种不稳定、易分解的酸,请写出该反应的化学方程式:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体.实验室由芳香化合物A制备H的一种合成路线如下: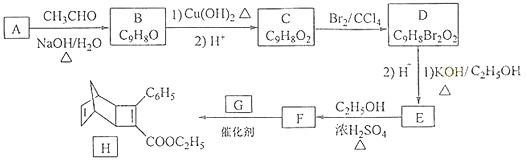
已知:①RCHO+CH3CHO ![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
② ![]() +
+ ![]()
![]()
![]()
回答下列问题:
(1)A的化学名称为为 .
(2)由C生成D和E生成F的反应类型分别为、 .
(3)E的结构简式为 .
(4)G为甲苯的同分异构体,由F生成H的化学方程式为 .
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2 , 其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,写出2种符合要求的X的结构简式 .
(6)写出用环戊烷和2﹣丁炔为原料制备化合物 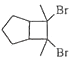 的合成路线(其他试剂任选).
的合成路线(其他试剂任选).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识填空.
(1)在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为(填序号) .
A.9
B.13
C.11~13之间
D.9~11之间
(2)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号) .
A.氨水与氯化铵发生化学反应
B.氯化铵溶液水解显酸性,增加了c(H+)
C.氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH﹣)减小
(3)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
①和两种粒子的物质的量之和等于0.1mol.
②和两种粒子的物质的量之和比OH﹣多0.05mol.
(4)已知某溶液中只存在OH﹣、H+、NH4+、Cl﹣四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl﹣)>c(NH4+)>c(H+)>c(OH﹣)
B.c(Cl﹣)>c(NH4+)>c(OH﹣)>c(H+)
C.c(Cl﹣)>c(H+)>c(NH4+)>c(OH﹣)
D.c(NH4+)>c(Cl﹣)>c(OH﹣)>c(H+)
①若溶液中只溶解了一种溶质,该溶质的名称是 , 上述离子浓度大小顺序关系中正确的是(选填序号) .
②若上述关系中C是正确的,则溶液中溶质的化学式是 .
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)c(NH3H2O)(填“>”、“<”、或“=).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生产生活中,我们会遇到各种各样的化学反应。请按要求回答下列问题:
(1)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、N2、Fe2O3、Fe、FeCl3 和 X。
①根据题意,可判断出X是_____________(写化学式)
②写出并配平该反应的化学方程式,并用双线桥标出电子转移的方向和数目:______。
(2)铝元素是自然界中含量最多的的金属元素,应用广泛。金属铝既能与酸反应又能与强碱反应,请写出铝与强碱反应的离子方程式__________________________________________ 。
(3)Na2O2可用作呼吸面具的供氧剂, 发生反应的化学方程式为__________________________。
(4)“水玻璃”长期暴露在空气中会变质,这是因为“水玻璃”与空气中少量二氧化碳接触,生成了乳白色的凝胶状沉淀的缘故。写出反应的离子方程式_________________________________。
(5)小苏打可作胃药,请写出其中和胃酸时的离子方程式______________________ 。
(6)在反应 3BrF3+5H2O = HBrO3+Br2+9HF+O2 中,被氧化的元素是____________,当有5 mol水反应时,由H2O还原的BrF3为______________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com