
| 阳离子 | K+ NH4+ Fe2+ Mg2+ Al3+ Cu2+ |
| 阴离子 | OH- Cl- Al02- CO32- SiO32-SO42- |
| A. | 原溶液中只含有NH4+ Fe2+Cl- SO42- | |
| B. | 由沉淀A推断原溶液中一定含有SO42- | |
| C. | 滤液A中可能含有K+ Al3+ Cl- | |
| D. | 沉淀B中一定含有Mg(OH)2 |
分析 某溶液中只含如表离子中的几种(不考虑水的电离与离子水解),且各离子的物质的量浓度均为0.1mol/L,
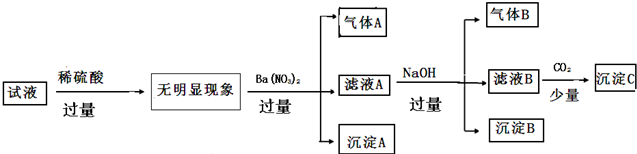
试液中加入过量稀硫酸没有明显现象,说明溶液中不含Al02-、CO32-、SiO32-,然后向溶液中加入过量硝酸钡溶液产生气体A,酸性条件下硝酸根离子具有氧化性,能氧化还原性离子,A为NO,则原溶液中含有Fe2+,则原溶液中不含OH-;
滤液A中加入过量NaOH,产生气体B,B为氨气,则原溶液中含有NH4+;
各种离子的物质的量浓度均为0.1mol•L-1,已经确定含有的阳离子为Fe2+、NH4+,而阴离子只能含有Cl-、SO42-,结合电荷守恒可知溶液中一定不存在K+、Mg2+、Al3+、Cu2+,所以沉淀B为氢氧化铁,滤液B中含有氢氧化钡,通入二氧化碳后生成了沉淀C碳酸钡,
据此分析解答.
解答 解:某溶液中只含如表离子中的几种(不考虑水的电离与离子水解),且各离子的物质的量浓度均为0.1mol/L,
试液中加入过量稀硫酸没有明显现象,说明溶液中不含Al02-、CO32-、SiO32-,然后向溶液中加入过量硝酸钡溶液产生气体A,酸性条件下硝酸根离子具有氧化性,能氧化还原性离子,A为NO,则原溶液中含有Fe2+,则原溶液中不含OH-;
滤液A中加入过量NaOH,产生气体B,B为氨气,则原溶液中含有NH4+;
各种离子的物质的量浓度均为0.1mol•L-1,已经确定含有的阳离子为Fe2+、NH4+,而阴离子只能含有Cl-、SO42-,结合电荷守恒可知溶液中一定不存在K+、Mg2+、Al3+、Cu2+,所以沉淀B为氢氧化铁,滤液B中含有氢氧化钡,通入二氧化碳后生成了沉淀C碳酸钡,
A.通过以上分析知,原溶液中只含有NH4+、Fe2+、Cl-、SO42-,故A正确;
B.由于开始时加入了稀硫酸,通过沉淀A无法判断原溶液中是否含有SO42-,故B错误;
C.滤液A中含有Cl-,但一定不存在K+、Al3+,故C错误;
D.根据分析可知,沉淀B为碳酸钡,原溶液中一定不存在镁离子,故D错误;
故选A.
点评 本题以离子检验为载体考查物质检验和鉴别,为高频考点,明确常见离子的性质为解答关键,注意掌握常见离子的检验方法及其现象,根据电荷守恒判断离子的组成情况为易错点,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
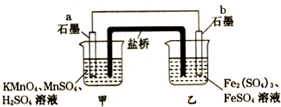 设计如图原电池(2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O),盐桥中装有饱和溶液.下列说法正确的是( )
设计如图原电池(2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O),盐桥中装有饱和溶液.下列说法正确的是( )| A. | 外电路电子的流向是从a到b | |
| B. | 电池工作时,盐桥中的SO42-移向甲烧杯 | |
| C. | a电极上发生的反应为:MnO4-+8H++5e-═Mn2++4H2O | |
| D. | 双液原电池工作时产生大量的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱电解质 | H2CO3 | NH3•H2O |
| Ka1 | 4.30×10-7 | 1.77×10-5 |
| Ka2 | 5.61×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①③④ | C. | ③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ①②④⑤ | C. | ①③⑤ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
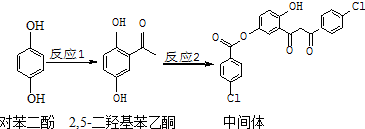
| A. | 对苯二酚在空气中能稳定存在 | |
| B. | 1 mol该中间体最多可与11 mol H2反应 | |
| C. | 2,5-二羟基苯乙酮能发生加成、取代、缩聚反应 | |
| D. | 该中间体分子中含有1个手性碳原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com