
| A. | 丁酸 | B. | 丁烯(C4H8) | C. | 二氯丁烷 | D. | 丁醇 |
分析 A.丁酸属于酸的同分异构体有正丁酸和异丁酸两种结构;
B.丁烯存在官能团位置异构和碳链异构,还有种类异构;
C.丁烷中,存在碳链为C-C-C-C和异丁烷两种,判断氯原子在同个碳上时和氯在不同碳上时的二氯代物种数;
D.丁醇的分子式为C4H100,减去官能团-OH,剩下的烃基为C4H9-,先判断烃基的种类数目,再插入羟基;
解答 解:A.丁酸属于酸的同分异构体有正丁酸和异丁酸两种结构,故A有2种同分异构体;
B.丁烯存在官能团位置异构和碳链异构,没有支链时,丁烯有1-丁烯而2-丁烯两种,当有一个支链时,有异丁烯1种结构,故B共3种;
C.丁烷中,当碳链为C-C-C-C,氯原子在同个碳上时,有2种结构,氯在不同碳上时,有4种结构;当为异丁烷时,氯原子在同个碳上时,有1种结构,氯在不同碳上时,有2种结构,共2+4+1+2=9种二氯代物;
D.丁醇的分子式为C4H100,减去官能团-OH,剩下的烃基为C4H9-,直链烃C-C-C-C有两种H,故醇有2种结构,带支链的烃有2中H,对应的醇有2种,共4种醇;
故选C.
点评 本题考查了同分异构体数目的求算,题目难度中等,明确同分异构体的书写原则为解答关键,试题侧重考查学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:解答题
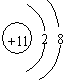 .
. ,所含的化学键类型为离子键、共价键.
,所含的化学键类型为离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
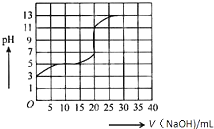 常温下,用0.50mol/L氢氧化钠溶液滴定某一元弱酸(HA)的溶液中,滴定曲线如图所示,下列叙述不正确的是( )
常温下,用0.50mol/L氢氧化钠溶液滴定某一元弱酸(HA)的溶液中,滴定曲线如图所示,下列叙述不正确的是( )| A. | 该弱酸在滴定前的浓度大于0.001mol/L | |
| B. | 由滴定起点数据可计算该弱酸的Ka(电离平衡常数)为2×10-5 | |
| C. | 滴定过程为求滴定终点,最合适的指示剂是酚酞 | |
| D. | 滴定终点时,c(Na+)>c(A-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度能加快反应速率 | |
| B. | 使用恰当的催化剂能加快反应速率 | |
| C. | 增大N2的浓度能加快反应速率 | |
| D. | 平衡时各组分含量之比一定等于3:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
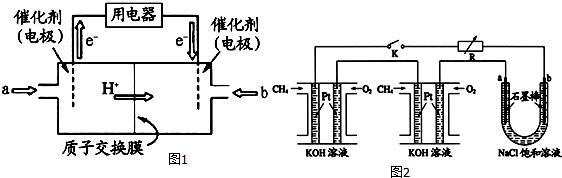
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
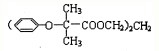 .已知:
.已知: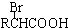 $\stackrel{苯酚钠}{→}$
$\stackrel{苯酚钠}{→}$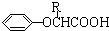
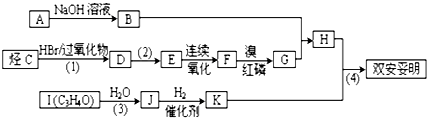
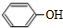 ,JHOCH2CH2CHO,C化学名称2-甲基-1-丙烯.
,JHOCH2CH2CHO,C化学名称2-甲基-1-丙烯.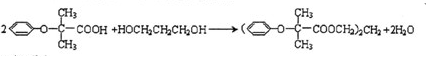 .
.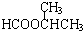 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
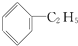 与
与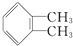
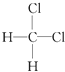 与
与
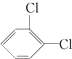 与
与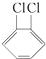
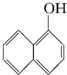 与
与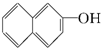
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L CO2与一定量的Na2O2反应转移的电子数目一定为0.1NA | |
| B. | C2H2、H2O2、Na2O2的最简式都可以用AB的形式表示 | |
| C. | 50 mL 12 mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| D. | 2.0 gH218O与D216O的混合物中所含中子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
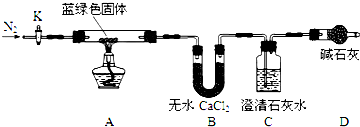
| 溶解度(S)/p | 溶度积(Ksp) | 摩尔质量(M)/g•mol-1 | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com