
某班同学用如下实验探究Na2CO3、NaHCO3的性质。回答下列问题:
(1)甲组同学分别取1.0g Na2CO3、NaHCO3固体,各滴加几滴水,发现盛Na2CO3的试管温度上升,而盛NaHCO3的试管温度下降;原因是______________。
(2)乙组同学分别取0.1mol/L Na2CO3、0.1mol/LNaHCO3的溶液,用0.1mol/LHCl溶液滴定,pH变化与盐酸体积的关系如图所示:
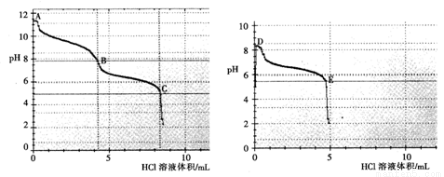
碳酸钠与盐酸反应pH有两次突变,达到两次反应终点,分别是__________(填A、B、C、D或E)。
B点的主要溶质是_____________(用化学式表示)。
③ B点__________(填“大于”或“小于”) D点的pH,主要原因是________________。
(3)丙组同学预测NaHCO3有酸性,向其溶液加入镁粉,发现有气泡和沉淀生成,写出化学方程式:_________________________。
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源:2016-2017学年河南省高二上第一次考试化学卷(解析版) 题型:选择题
下列反应既属于氧化还原反应,又属于放热反应的是
A.灼热的碳与二氧化碳的反应 B.盐酸与烧碱溶液的反应。
C.乙醇在空气中的燃烧 D.氢氧化钡晶体与氯化铵晶体在常温下的反应
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是( )
A.将铜插入稀硝酸中:Cu+4H++2NO3 -=Cu2++2NO2↑+H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe=2Fe3+
C.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3﹒H2O=Al(OH)3↓+3NH4+
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+3Na+
查看答案和解析>>
科目:高中化学 来源:2017届山东省滕州市高三上学期10月月考化学试卷(解析版) 题型:选择题
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g) +2CO(g) 2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其它条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其它条件不变,使用不同催化剂,该反应的平衡常数不变
查看答案和解析>>
科目:高中化学 来源:2017届山东省滕州市高三上学期10月月考化学试卷(解析版) 题型:选择题
①②③④ 四种金属片两两相连浸入稀硫酸中都可组成原电池 ,①②相连时,外电路电流从②流向① ;①③相连时,③为正极,②④相连时,②有气泡逸出 ;③④ 相连时,③ 的质量减少 ,据此判断这四种金属活动性由大到小的顺序是 ( )
A. ①③②④ B. ③④②① C.①③④② D.③①②④
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期第一次联考化学试卷(解析版) 题型:选择题
0.1molCu、0.lmolH2SO4、0.1lmolHNO3混合共1L,充分反应,下列预测正确的是
A.铜全部溶解,且溶液为蓝色,有红棕色气体产生
B.铜部分溶解,且溶液为蓝色,有红棕色气体产生
C.铜全部溶解,且溶液为蓝色,有无色气体产生
D.铜部分溶解,且溶液为蓝色,有无色气体产生
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期第一次联考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数值,下列有关叙述正确的是
A.28gMgCO3和NaHCO3混合固体中的CO32-离子数为NA
B. lmolI2与4molH2反应生成的HI分子数为2NA
C. 1molAl溶于含1molNaOH溶液,电子转移数为3NA
D. 标准状况下,2.24LH2O含有的共价键数为0.2NA
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三上第二次模拟化学试卷(解析版) 题型:选择题
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子是外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是 ( )
A. 元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
B. 元素X不能与元素Y形成化合物X2Y2
C. 元素Y、R分别与元素X形成的氢合物的热稳定性:XmY>XmR
D. 元素W、R的最高价氧化物的水化物都是强酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上第一次月考化学卷(解析版) 题型:填空题
顺-1,2-二甲基环丙烷和反-1,2-二甲基环丙烷可发生如下转化:
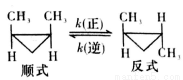
该反应的速率方程可表示为:v(正)=k(正)c(顺)和v(逆)=k(逆)c(反),k(正)和k(逆)在一定温度时为常数,分别称作正,逆反应速率常数。
回答下列问题:
(1)已知:T1温度下,k(正)=0.006s-1,k(逆)=0.002s-1,该温度下反应的平衡常数值K1 =__________;该反应的活化能Ea (正)小于Ea (逆),则∆H_________0(填“小于”“等于”或“大于”)。
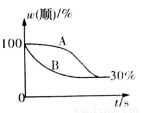
(2)T2温度下,图中能表示顺式异构体的质量分数随时间变化的曲线是___________(填曲线编号),平衡常数值K2 =__________;温度T2_________T1 (填“小于”“等于”或“大于”),判断理由是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com