
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铁钉放入氯化铁溶液中 |
| A. | 实验①和③中的铁钉只作还原剂 | |
| B. | 上述实验证明氧化性:Fe3+>Fe2+>Cu2+ | |
| C. | 实验②中,当转移0.2mol电子时,有0.1mol的Fe2+被氧化 | |
| D. | 实验③中反应的离子方程式为:Fe+Fe3+═2Fe2+ |
分析 ①中发生反应:Fe+Cu2+═Fe2++Cu,②中发生反应:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O,③中发生反应:Fe+2Fe3+═3Fe2+,结合元素的化合价升降及氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性来解答.
解答 解:A.实验①和③中发生氧化还原反应,单质铁中Fe元素的化合价升高,则都只作还原剂,故A正确;
B.由氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性可知,氧化性为Fe3+>Cu2+>Fe2+,故B错误;
C.实验②中发生反应3Fe2++4H++NO3-═3Fe3++NO↑+2H2O,根据电子守恒,被氧化的Fe2+的物质的量为:$\frac{0.2mol}{3-2}$=0.1mol,故C错误;
D.实验③中反应的离子方程式为:Fe+2Fe3+═3Fe2+,故D错误;
故选A.
点评 本题考查氧化还原反应,题目难度不大,明确发生的氧化还原反应及反应中元素的化合价变化是解答本题的关键,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| B. | 工艺师利用盐酸刻蚀石英制作艺术品 | |
| C. | 二氧化硅可用于制备光导纤维 | |
| D. | 化学家采用玛瑙研砵磨擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 天然气是 理想的洁净能源 | |
| B. | 燃烧天然气产生的有害废气比氢气少 | |
| C. | 用天然气作燃料可解决温室效应问题 | |
| D. | 天然气、沼气的主要成分都是CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔分子的结构式:H-C≡C-H | B. | 苯的结构简式: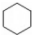 | ||
| C. | 乙醛分子的结构简式:CH3COH | D. | 甲烷分子的比例模型: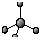 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol/L CuCl2溶液中含有的Cl-的个数为2NA | |
| B. | 16 g甲烷中含有的共用电子对数为NA | |
| C. | 常温常压,46 gNO2与N2O4的混合气体中含有的原子数为3NA | |
| D. | 4.6 g Na与适量氧气完全反应生成Na2O、Na2O2的混合物中含有的阴离子数大于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
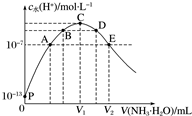 常温下向25mL盐酸中逐滴滴入0.1mol•L-1氨水,溶液中由水电离出的c水(H+)随滴入氨水的体积变化如图所示.
常温下向25mL盐酸中逐滴滴入0.1mol•L-1氨水,溶液中由水电离出的c水(H+)随滴入氨水的体积变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径 A>B>D>C | B. | 原子序数 D>C>B>A | ||
| C. | 离子半径 C>D>B>A | D. | 单质的还原性 A>B>D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com