


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
| A、2.3克金属钠变为钠离子失去的电子数目为0.1NA |
| B、18克水所含有的电子数目为NA |
| C、在常温常压下,11.2L氯气所含的原子数目为NA |
| D、2.8克氯气和一氧化碳混合气体的原子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
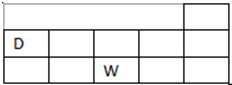
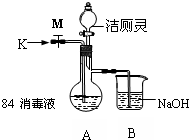
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用规格为10mL的量筒量取6.2mL的液体 |
| B、用蒸发方法使NaCl从溶液中析出时,应边加热边搅拌直至溶液完全蒸干 |
| C、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| D、制取蒸馏水时,冷凝管中冷凝水应由下口进,上口出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阳极上产生0.025mol的O2 |
| B、电解过程中总共转移0.2mol的电子 |
| C、所得溶液中的C(H+)=0.3mol/L |
| D、阴极增重1.08g |
查看答案和解析>>
科目:高中化学 来源: 题型:
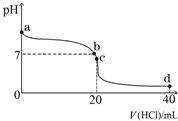 (1)有下列物质 ①Cu;②液氨;③CH3COOH;④NaHCO3;⑤H2O;⑥熔融NaCl;⑦NH3?H2O;⑧NH4Cl属于弱电解质的是
(1)有下列物质 ①Cu;②液氨;③CH3COOH;④NaHCO3;⑤H2O;⑥熔融NaCl;⑦NH3?H2O;⑧NH4Cl属于弱电解质的是| 化学式 | NH3?H2O | HCN | CH3COOH | H2CO3 |
| 电离平衡常数(25℃) | Kb=1.77×10-5 | Ka=4.93×10-10 | Ka=1.76×10-5 | Ka1=4.30×10-7 Ka2=5.61×10-11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com