
| A. | Na2O | B. | H2O2 | C. | CH4 | D. | NaOH |
科目:高中化学 来源: 题型:实验题
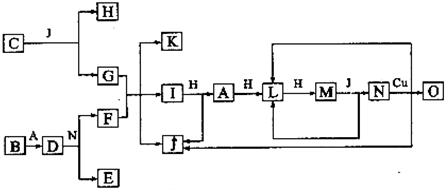
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
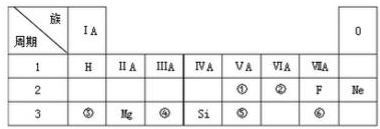
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
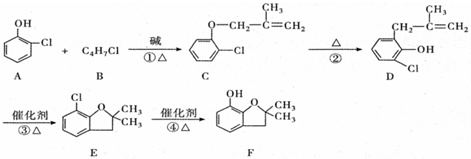
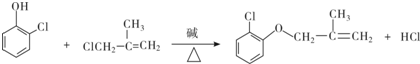 (有机物用结构简式表示,下同).
(有机物用结构简式表示,下同).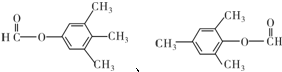
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
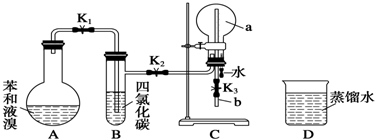
 ,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.
,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 36mol | B. | 20mol | C. | 16mol | D. | 20NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4、H2O、O2 |
| ② | Cl2、FeBr2 | FeCl3、Br2 |
| ③ | KMnO4、HCl | Cl2、MnCl2 |
| A. | 第①组反应中,H2O2作还原剂 | |
| B. | 第②组反应中,Cl2与FeBr2的物质的量之比可能为3:2 | |
| C. | 第③组反应中,每生成1mol Cl2转移电子2mol | |
| D. | 从三个反应可以得出:氧化性由强到弱顺序为MnO4->Fe3+>Cl2>Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com