
科目:高中化学 来源:不详 题型:单选题
| A.所有的原子核内质子数都比中子数多 |
| B.氢离子(H+)实质上是一个裸露的质子 |
| C.核外电子排布相同的微粒,其化学性质也相同 |
| D.非金属元素原子最外层电子数都大于4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.(水晶)SiO2 | B.冰醋酸 | C.氧化镁 | D.白磷 E.固体氩 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


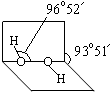
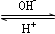 R(OH)3
R(OH)3 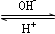 [R(OH)4]-
[R(OH)4]-查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.固体的热稳定性:Na2CO3>CaCO3>NaHCO3 |
| B.微粒半径:Fe(OH)3胶粒>K+>C1->Na+ |
| C.电离出氢离子的能力:CH3COOH>C2H5OH>H2O |
| D.氢化物的沸点:H2Se>H2S>H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com