
在标准状况下15 g CO与CO2的混合气体,体积为11.2 L。则:
(1)混合气体的密度是________________________________________________________________________。
(2)混合气体的平均摩尔质量是________________________________________________________________________。
(3)CO2和CO的体积之比是________________________________________________________________________。
(4)CO的体积分数是________________________________________________________________________。
(5)CO2和CO的质量之比是________________________________________________________________________。
(6)CO的质量分数是________________________________________________________________________。
(7)混合气体中所含氧原子的物质的量是________________________________________________________________________。
(8)混合气体中所含碳原子的物质的量是________________________________________________________________________。
答案 (1)1.339 g·L-1 (2)30 g·mol-1 (3)1∶7 (4)87.5% (5)11∶49 (6)81.7% (7)0.562 5 mol (8)0.5 mol
解析 (1)密度=质量/体积=15 g/11.2 L≈1.339 g·L-1。
(2)解法一:n=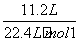 =0.5 mol,M=m/n=15 g/0.5 mol=30 g·mol-1。
=0.5 mol,M=m/n=15 g/0.5 mol=30 g·mol-1。
解法二:M=ρ·Vm=1.339 g·L-1×22.4 L·mol-1=30 g·mol-1。
(3)根据阿伏加德罗定律:体积之比=物质的量之比,最简单的方法是用十字交叉法计算:
30CO2 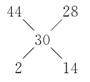 CO14
CO14
n(CO2)/n(CO)=1/7。
(4)CO的体积分数=CO的物质的量分数=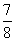 ×100%=87.5%。
×100%=87.5%。
(5)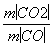 =
=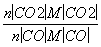 =
=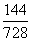 =11∶49。
=11∶49。
(6)CO的质量分数=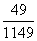 ×100%≈81.7%。
×100%≈81.7%。
(7)n(O)=2n(CO2)+n(CO)=2×0.5 mol×1/8+0.5 mol×7/8=0.562 5 mol。
(8)n(C)=n(CO2)+n(CO)=0.5 mol。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列物质中,不含离子键的是( )
①NH4HCO3 ②NH3 ③BaSO4 ④CuSO4·5H2O ⑤Ba(OH)2 ⑥H2SO4
A.①④⑥ B.②③⑤
C.④⑤ D.②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
在两个密闭容器中,分别充有质量相等的甲、乙两种气体,它们的温度和密度均相同。根据甲、乙的摩尔质量(M)的关系判断,下列说法中正确的是( )
A.若M(甲)<M(乙),则分子数:甲<乙
B.若M(甲)>M(乙),则气体摩尔体积:甲<乙
C.若M(甲)<M(乙),则气体的压强:甲>乙
D.若M(甲)>M(乙),则气体的体积:甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
某种元素原子的质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法不正确的是( )
A.由已知信息可得NA=
B.W g该原子的物质的量一定是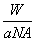 mol
mol
C.W g该原子中含有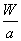 个该原子
个该原子
D.该原子的摩尔质量是aNA g
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.0.1 mol N2与足量的H2反应,转移的电子数是0.6NA
B.常温下,0.1 mol·L-1 NH4NO3溶液中含有的氮原子数是0.2NA
C.常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA
D.2.24 L CO和CO2的混合气体中所含的碳原子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下,将V L A气体(摩尔质量为M g·mol-1)溶于0.1 L水中,所得溶液的密度为ρ g·cm-3,则此溶液的物质的量浓度(mol·L-1)为( )
A.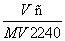 B.
B.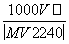
C.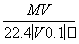 D.1 000VρM(MV+2 240)
D.1 000VρM(MV+2 240)
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在100 g浓度为c mol·L-1、密度为ρ g·cm-3的硫酸中加入一定量的水稀释成 mol·L-1的硫酸,则加入水的体积________ 100 mL(填“=”、“>”或“<”,下同)。
mol·L-1的硫酸,则加入水的体积________ 100 mL(填“=”、“>”或“<”,下同)。
(2)若把(1)中的H2SO4改成氨水,应加入水的体积________________________________________________________________________
100 mL。
(3)若把(1)(2)中的物质的量的浓度均改为溶质的质量分数,则加入水的体积________ 100 mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
把200 mL NH4HCO3和Na2CO3的混合溶液分成两等份,取一份加入含a mol NaOH的溶液恰好反应完全;取另一份加入含b mol HCl的盐酸恰好反应完全。该混合溶液中c(Na+)为( )
A.(10b-5a)mol·L-1 B.(2b-a)mol·L-1
C.( -
-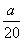 )mol·L-1 D.(5b-
)mol·L-1 D.(5b-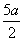 )mol·L-1
)mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.化学键的极性越大,键就越强
B.凡能形成氢键的物质,其熔、沸点比同类物质的熔、沸点高
C.CFH3分子中,既有H原子,又有电负性大、半径小的F原子,因此,CFH3分子间可以形成氢键
D.稀有气体能在温度充分降低时液化,而且随相对分子质量的增大熔点升高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com