
如图装置中,a、b试管内分别盛有食盐水和氯化铵溶液,各加入一块生铁片,放置一段时间。

下列有关描述错误的是
A.两块生铁片均发生电化学腐蚀
B.墨水柱两边的液面变为左低右高
C.两试管中相同的电极反应式为Fe - 2e-=Fe2+
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
科目:高中化学 来源:2014-2015吉林省松原市高二上学期期末化学试卷(解析版) 题型:选择题
如下图所示的实验。下列说法不正确的是

A.反应过程中产生的气泡是CO2 气体
B.加入石灰石的目的是为了促进氯化铁水解
C.最终所得红褐色液体为氢氧化铁胶体
D.反应过程中产生的气泡是HCl 气体
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省菏泽市高一上学期期末13校联考化学B试卷(解析版) 题型:填空题
(8分)一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+ Fe3+。
Fe3+。
在过程A中,Fe2+作 剂。
维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有 性。
(2)某些补铁剂的成分是硫酸亚铁,长期放置会因氧化而变质。检验硫酸亚铁是否变质的试剂是______________(填序号)。
①稀盐酸 ②石蕊溶液 ③KSCN溶液
(3)要除去FeCl3溶液中少量的氯化亚铁,可行的办法是 (填字母)。
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出该过程中发生反应的离子方程式 。
(4)电子工业常用30%的FeCl3 溶液腐蚀铜箔,制造印刷线路板,写出FeCl3 与金属铜反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省菏泽市高一上学期期末13校联考化学B试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.1 mol N2所含有的原子数为NA
B.标准状况下,22.4 L SO3中含有的分子数为NA
C.标准状况下,22.4 L氨气所含的原子数为NA
D.16 g O2和O3的混合气体所含的氧原子数为NA
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省菏泽市高二上学期期末13校联考化学B试卷(解析版) 题型:填空题
(6分)某氮肥厂氨氮废水中的氮元素多以 和NH3·H2O的形式存在,该废水的处理流程如下所示:
和NH3·H2O的形式存在,该废水的处理流程如下所示:

过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30 ℃,通空气将氨赶出并回收a.n
过程Ⅱ:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下图:

(1)第一步反应是_______________反应(选填“放热”或“吸热”),判断依据是__________。
(2)1 mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省菏泽市高二上学期期末13校联考化学B试卷(解析版) 题型:选择题
对于相同体积的K2CO3溶液(浓度为c1) 和 (NH4)2CO3溶液(浓度为c2),若其中CO的物质的量浓度相同,则c1和c2的关系是
A.c1=c2 B.c1<c2 C.c1≥c2 D.c1>c2
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省增城市高一上学期期末化学试卷(解析版) 题型:填空题
(16分)
高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,该物质广泛应用于日常生活用水和工业废水的处理。
(1)为检测PAFC中铝和铁元素的含量,采用如图所示流程进行。

回答下列问题:
①PAFC中铁元素的化合价为_________。
②步骤I中的试剂A是 (从“氢氧化钠溶液”、“氨水”中选择)
步骤Ⅲ中的试剂B是 。
③步骤Ⅱ的操作是 ,用到的主要玻璃仪器 。
(2)某工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:

①在废料中加入过量稀盐酸,发生多个离子反应,请在空白处补全离子方程式:
FeO+2H+ Fe2++H2O Al2O3+6H+
Fe2++H2O Al2O3+6H+ 2Al3++3H2O
2Al3++3H2O
Fe2O3+6H+ 2Fe3++3H2O
2Fe3++3H2O
②所得酸性溶液中,不能确定是否一定存在的阳离子是 (填序号)。
A.Al3+ B.Fe2+ C.Fe3+ D.H+
为证明该离子确实存在,可采用的操作(必须指明所采用的试剂及观察到的现象)是: 。
③往酸性溶液中加入试剂X的目的是(用离子方程式表示) 。
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省增城市高一上学期期末化学试卷(解析版) 题型:选择题
在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是
A.Na+、K+、OH-、Cl- B.Mg2+、Na+、SO 、Cl-
、Cl-
C.Ca2+、HCO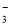 、NO
、NO 、K+ D.Na+、Cu2+、SO
、K+ D.Na+、Cu2+、SO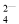 、NO
、NO
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省高一上学期期末考试化学试卷(解析版) 题型:选择题
化学与科技、社会、环境密切相关。下列有关说法正确的是
A.pH小于7的雨水被称为酸雨
B.明矾溶于水可产生具有吸附性的胶体粒子,常用于饮用水的杀菌消毒
C.推广使用燃煤脱硫技术,主要是为了防治SO2污染
D.PM2.5是指大气中直径小于或等于2.5微米(2.5×10-6m)的细小可吸入颗粒物,其与空气形成的分散系属于胶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com