

| A�� | ���������������٣��� | |
| B�� | �������������ʵ��������٣��� | |
| C�� | ��Һ��pH�仯�������ڼ�С | |
| D�� | �缫��Ӧʽ������������4OH--��2H2O+O2��+4e-������������2H++2e--��H2�� |
���� ������ӵ�Դ�������ǵ��أ�������ӦΪ2Cl--2e-=Cl2����������ӦΪ��Cu2++2e-=Cu����Ϊԭ��أ�������ӦΪ2H++2e-=H2����������ӦΪZn-2e-=Zn2+���Դ˽����⣮
��� �⣺A���ٵ�������Ӧ��2Cl--2e-=Cl2����������ͨ��0.02mol����ʱ���������������V=nVm=0.01mol��22.4L/mol=0.0224L�����е�������ӦΪ��2H++2e-=H2����������ͨ��0.02mol����ʱ���������������V=nVm=0.01mol��22.4L/mol=0.0224L�����Բ���������������=�ڣ���A����
B��������������ͭ����������������缫���������ʵ��������٣��ڣ���B��ȷ��
C�����൱�ڵ���Ȼ�ͭ����Һ��pH�������䣬���൱��п�������е������ӷ�Ӧ�����������Ӽ��٣����Լ���������pH����C����
D������������2Cl--2e-=Cl2�������е�������ӦΪ��2H++2e-=H2������D����
��ѡB��
���� ������һ���й�ԭ��غ͵��صĹ���ԭ�����ۺ���Ŀ��Ҫ��ѧ����Ϥ�̲Ļ���֪ʶ���߱������ͽ�������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe | B�� | O2 | C�� | H2O | D�� | H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��������������������л�ԭ�ԣ��ڿ������ױ�����Ϊ�������� | |
| B�� | ��״���£�ÿĦ������������ԼΪ2.24L | |
| C�� | ���������������������������� | |
| D�� | �����������Ư���ԡ������������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaHCO3��Һ | B�� | KSCN��Һ | C�� | NaOH��Һ | D�� | NH3•H2O��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
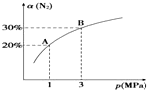 ij�¶��£����ڷ�ӦN2��g��+3H2��g��?2NH3��g����H=-92.4kJ•mol-1��N2��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
ij�¶��£����ڷ�ӦN2��g��+3H2��g��?2NH3��g����H=-92.4kJ•mol-1��N2��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ��1 mol������3 mol����������1 L�ܱ������з�����Ӧ���ų�������Ϊ92.4 kJ | |
| B�� | ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K��A����K��B�� | |
| C�� | ������Ӧ�ڴﵽƽ�������ѹǿ��H2��ת�������� | |
| D�� | �����¶ȣ�ƽ�����淴Ӧ�����ƶ���˵���淴Ӧ������������Ӧ���ʼ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ﶼ��������������Һ��Ӧ | |
| B�� | �����ڼ���ʱ���ܸ�������Ӧ | |
| C�� | �����ﶼ������ˮ������Ӧ���� | |
| D�� | ̼�趼��ͬ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H-+OH+=H2O | B�� | H++OH+=H2O | C�� | H-+OH-=H2O | D�� | H++OH-=H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| �� | �� | ||
| �� | �� | ||
| �� |
| A�� | ԭ�Ӱ뾶���ף��� | |
| B�� | �������ԭ�Ӻ�����������8 | |
| C�� | ����������Ӧ��ˮ��������ԣ������� | |
| D�� | �ĵ����ڿ�����ȼ������ֻ�����ۼ��Ļ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com