
 表示的分子式C6H14;名称是2-甲基戊烷.
表示的分子式C6H14;名称是2-甲基戊烷.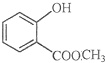 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.分析 (1)根据该有机物的键线式写出分子式,根据系统命名法完成该有机物的命名;
(2)根据有机物的结构写出分子中含有的官能团;
(3)丁烷有2种同分异构体,共含4种H,去掉1个H剩余的部分为丁基.
解答 解:(1) ,分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,命名为:2-甲基戊烷,
,分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,命名为:2-甲基戊烷,
故答案为:C6H14; 2-甲基戊烷;
(2) 分子中含有官能团是羟基和酯基,
分子中含有官能团是羟基和酯基,
故答案为:羟基、酯基;
(3)根据碳原子数目由多到少的顺序,丁基的结构简式为:-CH2CH2CH2CH3,-CH(CH3)CH2CH3,-CH2CH(CH3)2,-C(CH3)3,
故答案为:-CH2CH2CH2CH3,-CH(CH3)CH2CH3,-CH2CH(CH3)2,-C(CH3)3.
点评 本题考查了有机物命名、官能团的判断,难度不大,要求学生了解烷烃的命名、苯的同系物的命名及简单的烃的衍生物的命名方法,熟练掌握常见的官能团名称.


科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光导纤维、聚酯纤维、棉花都属于高分子化合物 | |
| B. | 在大米酿酒的过程中,淀粉最后变成了单糖 | |
| C. | 泡沫灭火器中用的是苏打和硫酸铝 | |
| D. | 海轮外壳上镶入锌块,可减缓船体的腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的能量一定低于M的,Y的能量一定低于N的 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | Z和Y的总能量一定高于M和N的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
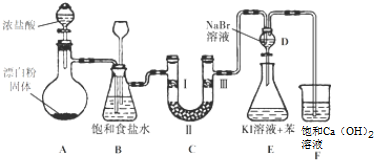
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:H2O<H2S<H2Se | B. | 微粒半径:K+>Na+>Mg2+>Al3+ | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D. | 熔点:Li>Na>K>Rb |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳溶于水生成碳酸,二氧化硅不溶于水也不能跟水直接反应生成硅酸 | |
| B. | 在高温条件下,二氧化硅跟碳酸钠反应,生成硅酸钠和二氧化碳 | |
| C. | 二氧化硅的熔点比二氧化碳高 | |
| D. | 二氧化碳通入Na2SiO3稀溶液中,生成白色胶状沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com