
【题目】下表是元素周期表的一部分. 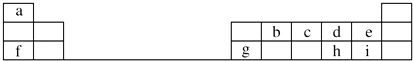
回答下列问题:
(1)元素b在元素周期表中的位置是 .
(2)元素a与c形成的4核10电子分子的化学式为 , 其水溶液呈性.
(3)元素e的负一价离子的结构示意图为 , 元素g的简单离子的结构示意图为 , 二者的离子半径大小顺序为 .
(4)元素i的气态氢化物比元素e的气态氢化物(填“稳定”或“不稳定”).
(5)元素i的单质溶于元素f的最高价氧化物对应的水化物中,可生成具有漂白作用的一种盐,该盐的电子式为 , 该化合物中所含的化学键类型为 .
(6)元素d与h形成的化合物的化学式为
【答案】
(1)第二周期ⅣA族
(2)NH3;碱
(3)![]() ;
;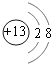 ;F﹣>Al3+
;F﹣>Al3+
(4)不稳定
(5)![]() ;离子键、共价键
;离子键、共价键
(6)SO2、SO3
【解析】解:由元素在周期表中位置,可知a为H、b为C、c为N、d为O、e为F、f为Na、g为Al、h为S、i为Cl.
(1.)由位置可知,b处于周期表中第二周期ⅣA族,所以答案是:第二周期ⅣA族;
(2.)元素a与c形成的4核10电子分子为NH3 , 氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而导致其水溶液呈碱性,所以答案是:NH3;碱性;
(3.)F﹣离子质子数为9,核外有2电子层,各层电子数为2、8,离子结构示意图为 ![]() ,Al3+离子质子数为13,核外有2电子层,各层电子数为2、8,离子结构示意图为
,Al3+离子质子数为13,核外有2电子层,各层电子数为2、8,离子结构示意图为 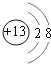 ,
,
F﹣、Al3+ , 离子电子层结构相同,核电荷数越大离子半径越小,故离子半径:F﹣>Al3+ , 所以答案是: ![]() ;
; 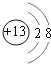 ;F﹣>Al3+;
;F﹣>Al3+;
(4.)非金属性Cl<F,元素非金属性越强,其氢化物越稳定,故HCl不如HF稳定,所以答案是:不稳定;
(5.)氯气单质溶于NaOH中生成具有漂白作用的盐为NaClO,由钠离子与次氯酸根离子构成,次氯酸根离子中氧原子与氯原子之间形成1对共用电子对,电子式为 ![]() ,含有离子键、共价键,所以答案是:
,含有离子键、共价键,所以答案是: ![]() ;离子键、共价键;(6)元素d与h形成的化合物有二氧化硫、三氧化硫,相应的化学式为SO2、SO3 , 所以答案是:SO2、SO3 .
;离子键、共价键;(6)元素d与h形成的化合物有二氧化硫、三氧化硫,相应的化学式为SO2、SO3 , 所以答案是:SO2、SO3 .


科目:高中化学 来源: 题型:
【题目】脂类是人体必需的营养成分之一,它的作用是( )
①构成细胞膜的一种成分 ②促进糖类代谢 ③备用能源物质 ④参与一切生命活动 ⑤提供能量 ⑥促进神经系统的正常功能
A.①②③
B.①③⑤
C.③⑤⑥
D.①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的表达正确的是( )
A.原子核内有10个中子的氧原子: ![]() O
O
B.氯原子的结构示意图: ![]()
C.Fe3+的最外层电子排布式为:3s23p63d5
D.基态铜原子的外围电子排布图: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。下列关于N4分子说法正确的是( )
A. N4属于一种新型的化合物B. N4沸点比P4(白磷)高
C. N4与N2互为同素异形体D. N4分子中存在离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机化学反应方程式及反应类型均正确的是( )
选项 | 化学反应方程式 | 反应类型 |
A | CH3COOH+CH3CH2OH | 酯化反应 |
B | CH4+Cl2 | 置换反应 |
C | CH2=CH2+Br2→CH3CHBr2 | 加成反应 |
D |
| 取代反应 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 镭是元素周期表中第ⅡA族元素,下列关于镭的叙述不正确的是
A. 镭比钙的金属性更强 B. 在化合物中呈+2价
C. 镭是一种放射性元素 D. 氢氧化镭呈两性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知MnO2与浓盐酸可以发生如下反应: 4HCl(浓)+MnO2 ![]() MnCl2+Cl2↑+2H2O,若产生7.1gCl2 , 则:
MnCl2+Cl2↑+2H2O,若产生7.1gCl2 , 则:
(1)参加反应的HCl是多少克?
(2)被氧化的HCl是多少克?
(3)参加反应的MnO2物质的量是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素A,B,C,D分别位于三个不同短周期,且原子序数依次增大.只有D为金属元素,它们可形成x、y、z、w四种常见的二元化合物及p、q两种常见三元化合物,它们之间存在如下转化关系;①x ![]() p
p ![]() q+z,②y
q+z,②y ![]() p+O2↑,其中z为液体、w为气体,其余均为固体.下列有关说法正确的是( )
p+O2↑,其中z为液体、w为气体,其余均为固体.下列有关说法正确的是( )
A.原子半径大小顺序:D>C>B>A
B.y、p 中均只含有离子键
C.B,D两元素最高价氧化物对应水化物分别为强酸、强碱
D.p能抑制水的电离而q能促进水的电离
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com