
【题目】根据图示回答下列问题:
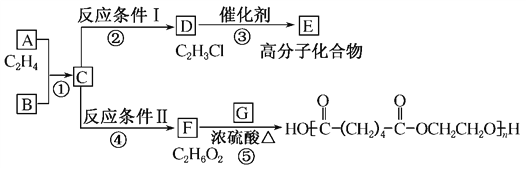
(1)写出A、E、G的结构简式:A________,E________,G________。
(2)反应②的化学方程式(包括反应条件)是_________________________,反应④的化学方程式(包括反应条件)是________________________。
(3)写出①、③、⑤的化学方程式及反应类型:
①___________________________________________________;
③___________________________________________________;
⑤___________________________________________________。
【答案】 CH2=CH2 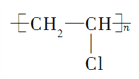 HOOC(CH2)4COOH )ClCH2CH2Cl+NaOH
HOOC(CH2)4COOH )ClCH2CH2Cl+NaOH![]() CH2=CHCl+NaCl+H2O ClCH2CH2Cl+2NaOH
CH2=CHCl+NaCl+H2O ClCH2CH2Cl+2NaOH![]() HOCH2CH2OH+2NaCl CH2=CH2+Cl2―→ClCH2CH2Cl加成反应
HOCH2CH2OH+2NaCl CH2=CH2+Cl2―→ClCH2CH2Cl加成反应 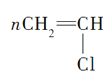
![]()
 加聚反应
加聚反应 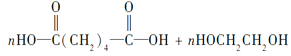
![]()
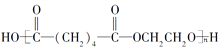 +(2n-1)H2O缩聚反应
+(2n-1)H2O缩聚反应
【解析】本题主要考查卤代烃的性质。
(1)A、E、G分别是乙烯、聚氯乙烯、己二酸,它们的结构简式:A CH2=CH2,E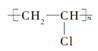 ,G HOOC(CH2)4COOH。
,G HOOC(CH2)4COOH。
(2)C是1,2-二氯乙烷,反应②发生卤代烃1,2—二氯乙烷的消去反应,反应的化学方程式(包括反应条件)是ClCH2CH2Cl+NaOH![]() CH2=CHCl+NaCl+H2O,反应④发生卤代烃1,2-二氯乙烷的水解反应,反应的化学方程式(包括反应条件)是ClCH2CH2Cl+2NaOH
CH2=CHCl+NaCl+H2O,反应④发生卤代烃1,2-二氯乙烷的水解反应,反应的化学方程式(包括反应条件)是ClCH2CH2Cl+2NaOH![]() HOCH2CH2OH+2NaCl。
HOCH2CH2OH+2NaCl。
(3)①、③、⑤的化学方程式及反应类型:
①CH2=CH2+Cl2―→ClCH2CH2Cl,加成反应,③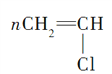
![]()
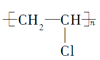 ,加聚反应,
,加聚反应,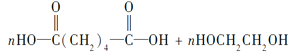
![]()
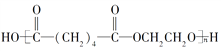 +(2n-1)H2O,缩聚反应。
+(2n-1)H2O,缩聚反应。


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】工业上,若输送Cl2的管道漏气,用NH3进行检验时生成NH4Cl和N2 . 下列说法正确的是( )
A.元素H只有 ![]() H和
H和 ![]() H两种核素
H两种核素
B.Cl2 , NH4Cl中氯元素微粒的半径:r(Cl)>r(Cl﹣)
C.工业上常用干燥的钢瓶储存液氯,是因为铁和氯气在任何条件下都不反应
D.该反应表明常温下氯气有氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据表中的信息判断下列说法正确的是( )
物质 | 金刚石 | 石墨 |
外观 | 无色,透明固体 | 灰黑,不透明固体 |
熔点 | ? | ? |
燃烧热/KJmol﹣1 | 395.4 | 393.5 |
A.表示石墨燃烧热的热化学方程式为C(石墨,s)+ ![]() ?O2(g)═CO(g)△H=﹣393.5 kJ?mol﹣1
?O2(g)═CO(g)△H=﹣393.5 kJ?mol﹣1
B.由表中信息知C(石墨,s)═C(金刚石,s)△H=+1.9 kJ?mol﹣1
C.由表中信息可得如图所示的图象 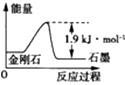
D.由表中信息可推知相同条件下金刚石的熔点高于石墨的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D,E,F六种化合物,其中A,B,C,D,E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成.B、C的组成元素相同,且C的摩尔质量比B大80g/mol,回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为
A.离子键
B.极性共价键
C.非极性共价键
D.氢键
(2)下表为B与F实验的部分内容
①在含B的溶液中加入稀H2SO4 , 产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
写出B与稀H2SO4反应的离子方程式
写出②中反应的化学方程式
(3)现由6种粒子Mn2+、MnO ![]() 、H+、H2O、X2Y
、H+、H2O、X2Y ![]() (C中含有的阴离子),XY
(C中含有的阴离子),XY ![]() 完成一个离子方程式,已知Mn2+为还原剂,得到1molMnO
完成一个离子方程式,已知Mn2+为还原剂,得到1molMnO ![]() 需氧化剂的物质的量为mol
需氧化剂的物质的量为mol
(4)化合物D和E相互转化D ![]() E,若有D和ExH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为g,ExH2O的化学式为 .
E,若有D和ExH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为g,ExH2O的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.某兴趣小组的实验数值结果大于57.3kJmol﹣1(中和热),原因可能是( ) 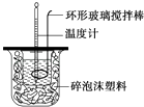
A.实验装置中小烧杯杯中低于大烧杯杯口
B.用浓硫酸代替了稀硫酸
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后未洗涤,直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A.已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定
B.氢气的燃烧热为285.5 kJmol﹣1 , 则水分解的热化学方程式2H2O(l)=2H2(g)+O2(g)△H=+285.5 kJmol﹣1
C.已知稀溶液中,H+(aq)+OH﹣(aq)=H2O(l)△H=﹣57.3 kJmol﹣1 , 则浓硫酸与稀NaOH溶液反应生成1 mol水时放出的热量为57.3 kJ
D.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量.则Fe(s)+S(s)=FeS(s)△H=﹣95.6 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被称为万能还原剂的 NaBH4 溶于水并和水反应: NaBH4+2H2O=NaBO2+4H2↑。下列说法中正确的是(NaBH4 中 H 为-1 价)
A. NaBH4 既是氧化剂又是还原剂 B. NaBH4 是氧化剂,H2O 是还原剂
C. 硼元素被氧化,氢元素被还原 D. 被氧化的元素与被还原的元素质量之比为 1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com