
【题目】下列说法正确的是( )
A.反应热是1 mol物质参加反应时的能量变化
B.当反应放热时ΔH>0,反应吸热时ΔH<0
C.任何条件下,化学反应的焓变都等于化学反应的反应热
D.在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物的焓的差值来决定
科目:高中化学 来源: 题型:
【题目】已知1g氢气完全燃烧生成水蒸气时放出121kJ的能量,且氧气中1molO=O键完全断裂时需要吸收496kJ的能量,水蒸气中1mol H-O键形成时放出463kJ的能量,则氢气中1mol H-H键断裂时吸收的能量为
A.920kJ B.557kJ C.436kJ D.181kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验:
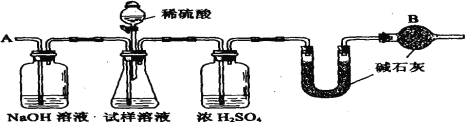
主要步骤如下:
①按图组装仪器,并检查装置的气密性
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U形管的重量,得到b g
④从分液漏斗滴入6mol·1-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓慢鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的重量,得到c g
⑦ 重复步骤⑤和⑥的操作一直到U型管的质量基本不变,为d g
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明
(2)装置中干燥管B的作用是
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果 (填偏高、偏低或不变)
(4)步骤⑤的目的是
(5)步骤⑦的目的是
(6)该试样中纯碱的质量分数的计算式为
(7)还可以用其他实验方法测定试样中纯碱的质量分数,请简述一种不同的实验方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分离提纯方法选择不正确的是
A | 除去氯化钠溶液中的泥沙 | 过滤 |
B | 用四氯化碳提取溴水中的溴 | 萃取 |
C | 分离乙酸(沸点 118℃ )与乙酸乙酯(沸点 77℃ ) | 分液 |
D | 从含有少量氯化钠的硝酸钾溶液中提取硝酸钾 | 结晶 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.放热反应在常温下一定很容易发生
C.物质发生化学反应一定伴随着能量变化
D.凡是吸热或放热过程中热量的变化均称为反应热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过分析比较,认为无需检验就可判断其中必有的两种物质是 和 。(填化学式)
(2)为了确定X,现将(1)中的两种物质记为A和B,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕色沉淀,向该沉淀中滴入稀硝酸,沉淀部分溶解,最后留有白色沉淀不再溶解。则:
①X为 。
A.SO32-B.SO42- C.CH3COO-D.SiO32-
②A中的化学键类型为
③将0.02mol的A与0.01mol的C同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的质量为 (精确到0.1g)。
④利用上述已经确定的物质,可以检验出D、E中的阳离子。请简述实验操作步骤、现象及结论
(3)将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀硫酸,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的 (填相应的离子符号)。有关反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物a的分子式和己烷相同,且主链上有4个碳原子,则下列关于a 的观点正确的是( )
A.a分子中可能有三个甲基
B.a的一氯代物可能有三种
C.a的分子式为C6H10
D.a能与溴的四氯化碳溶液发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述中正确的是( )
4NO(g)+6H2O(g),下列叙述中正确的是( )
A.达到化学平衡时4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达平衡状态
C.达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大
D.平衡混合物中各物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)某无色溶液样品中溶质可能含有NaOH和Na2SO4,某化学小组同学为了确认两种物质是否存在,设计并进行如下探究活动:
【探究方案设计】
为了确定NaOH的存在,设计了如下方案。
张南同学的方案:取溶液样品少许于试管中,向其中滴加无色酚酞溶液,即可确定溶液中溶质是否含NaOH;
小岗同学的方案:取溶液样品少许于试管中,向其中滴加稀盐酸,即可确定溶液中溶质是否含NaOH;
【交流讨论】
经过小组同学讨论认为小岗同学的方案不可以。
请你表明态度,并对小岗同学的方案进行评价(1)_____________________。由此得出结论,用化学实验的方法验证物质的存在,不仅所加试剂与被检验物质能发生化学反应,还需要(2)________,才能验证物质的存在;经过小组同学讨论后重新设计了整体方案,并进行了如下实验。
【探究实验】
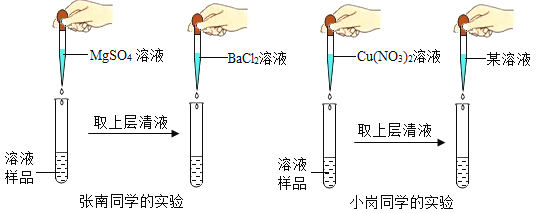
张南同学的实验:重新取溶液样品少许于试管中,向其中滴加足最MgSO4溶液,出现白色沉淀后,取上层清液,再滴加BaCl2溶液,又出现白色沉淀,确定溶液中溶质含NaOH和Na2SO4,请你对张南同学的实验及结论进行评价(3)___________________;小岗同学的实验:重新取溶液样品少许于试管中,其中滴加足量Cu(NO3)2溶液,出现(4) ____________(填实验现象)后,确定溶液中溶质含NaOH,反应的化学方程式为(5)____________;待上述沉淀完全后,取上层清液,再滴加(6) ____________溶液,出现白色沉淀,可确定溶液中溶质含Na2SO4,
【反思与总结】由此得出结论,用化学实验的方法验证同一溶液中两种物质的存在,不仅所加试剂与被检验物质能发生反应,还需要考虑所加试剂(7) ____________,才能验证这两种物质的存在。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com