
【题目】已知铅蓄电池的工作原理为Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。

(1)A是铅蓄电池的___________极,铅蓄电池正极反应式为___________,放电过程中电解液的密度___________ (填“减小”、“增大”或“不变”)。
(2)Ag电极的电极反应式是___________,该电极的电极产物共____________g。
(3)Cu电极的电极反应式是____________,CuSO4溶液的浓度____________(填“减小”、“增大”或“不变”)
(4)如图表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示___________。

a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
【答案】 负 PbO2+4H++SO42-+2e-=PbSO4+2H2O 减小 2H++2e-=H2↑ 0.4 Cu-2e-=Cu2+ 不变 B
【解析】试题分析:(1)当铅蓄电池中转移0.4mol电子时铁电极的质量减小11.2g,说明铁作阳极,银作阴极,阴极连接原电池负极,所以A是负极,B是正极,正极上二氧化铅得电子发生还原反应,电极反应式为PbO2+4H++SO42-+2e-═PbSO4+2H2O,放电过程中消耗硫酸,硫酸溶液的密度随浓度减小而减小,故电解的密度减小;
(2)银作阴极,电解稀硫酸时,阴极上氢离子放电生成氢气,电极反应式为2H++2e-═H2↑,生成氢气的质量=0.4mol/2×2g/mol=0.4g;
(3)铜作阳极,阳极上铜失电子发生氧化反应,电极反应式为Cu-2e-═Cu2+,阴极上析出铜,所以该装置是电镀池,电解质溶液中铜离子浓度不变;
(4)右边U形管不析出气体,左边U形管析出气体,所以稀硫酸析出气体体积大于硫酸铜溶液,a错误;当转移相等电子时,溶解金属的物质的量相等,铜的摩尔质量大于铁,所以右边U形管阳极减少的质量大于左边U形管阳极减少的质量,b正确;当转移相等电子时,析出物质的物质的量相等,但铜的摩尔质量大于氢气,所以左边U形管析出氢气的质量小于右边U形管析出铜的质量,c错误。


科目:高中化学 来源: 题型:
【题目】下列有机分子中,可形成顺反异构的是( )
A. CH2=CHCH3 B. CH2=CHCH2CH3
C. CH3CH=C(CH3)2 D. CH3CH=CHCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料,分子中碳与氢元素的质量比为6:1,,是同系物中最简单的物质。X为有浓郁香味、不易溶于水的油状液体。它们之间的转化关系如图:
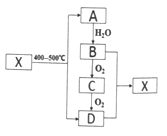
请回答:
(1)有机物D中含有的官能团名称是_________。
(2)A→B的反应类型是_______________。
(3)有机物X在400~500℃下转化为A和D的化学方程式是_____________________。
(4)下列说法正确的是_______________。
A.工业上获得A的的主要方法是催化裂化
B.将绿豆大小的钠投入到B中,钠块浮在液面上,并产生气泡
C.除去C中的D可以先加饱和碳酸钠溶液再蒸馏
D.一定条件下,1molX与足量NaOH溶液反应时,最多消耗1molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现含有NaCl、MgCl2、CaCl2的混合液,某同学欲提取纯净的NaCl晶体,设计了如下实验:

请回答下列问题:
(1)写出沉淀中所含物质的化学式_________,①中加入的过量试剂为_____。
(2)上述流程中,加入过量稀盐酸的目的是______________。
(3)操作I的名称是_____,操作Ⅱ的名称是_____。
(4)操作I的要点是一帖二低三靠,其中二低是指__________,____________。操作Ⅱ中当______(填仪器名称)中____________________________(填现象)时停止加热。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属单质根一定浓度的硝酸反应后,假定只产生单一的还原产物。当参加反应的金属单质与被还原的硝酸的物质的量之比为2:1时,还原产物可能为( )
A.NO2 B.NO C.N2O D.N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3Cl2+6NaOH==5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A. Cl2是氧化剂,NaOH是还原剂
B. 被氧化的Cl原子和被还原的Cl原子的物质的量之比为5∶1
C. Cl2既做氧化剂又做还原剂
D. 氧化剂得电子数与还原剂失电子数之比为5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.Na2O2+2HCl===2NaCl+H2O2
B.Ag2O+H2O2===2Ag+O2↑+H2O
C.2H2O2===2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH===2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2仅体现氧化性的反应是(填序号,下同)_________,H2O2既体现氧化性又体现还原性的反应是________。
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序是_____________
(3)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。
①写出上述反应的离子方程式并配平
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子为_______mol。
(4) H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应:KCN+H2O2+H2O===A+NH3↑,试指出生成物A的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为元素周期表中短周期的一部分,下列说法正确的是()

A. 非金属性:Y>Z>M
B. 离子半径:M->Z2->Y-
C. ZM2分子中各原子的最外层均满足8电子稳定结构
D. 三种元素中,Y的最高价氧化物对应的水化物酸性最强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com