
����Ŀ���������ȡ����Ӧ��ʵ��װ����ͼ��ʾ������AΪ��֧�Թܸ��Ƴɵķ�Ӧ�����������¶˿���һС�ף�����ʯ���ޣ��ټ���������м�� 
��1����д���пհף� ���Թ�A�еķ�Ӧ����ʽΪ
���Թ�C�����Ȼ�̼�������ǣ� �� ��Ӧ��ʼ�۲�D��E���Թܣ�����������ֱ�Ϊ��D�� �� E�� �� д��E�з�Ӧ�����ӷ���ʽ
�۷�Ӧ2��3min����B�е�NaOH��Һ��ɹ۲쵽�������� �� ԭ��
��2��ʵ�����Ʊ�����������Ҫ�������£� a������һ��������ŨH2SO4��ŨHNO3�Ļ���ᣬ���뷴Ӧ���У�
b���������µĻ��������μ���һ�����ı����������Ͼ��ȣ�
c����55��60���·�����Ӧ��ֱ����Ӧ������
d����ȥ�����ֲ�Ʒ����������ˮ��5%NaOH��Һϴ�ӣ������������ˮϴ�ӣ�
e��������ˮCaCl2�����Ĵ��������������õ�����������������д���пհף�
���Ʊ��������ķ�Ӧ������
������һ��������ŨH2SO4��ŨHNO3�Ļ����ʱ��������ע�������ǣ� ��
�۲���d��ϴ�ӡ������������Ӧʹ�õ�������
���𰸡�
��1�� ����ȥHBr�����л��е�������?? ���ջӷ����л�������ʯ����Һ������죬���ڵ��ܿ��а�������������dz��ɫ������Ag++Br���TAgBr��������Һ�ײ�����ɫ��״Һ�壻�屽�л������Ե��
����ȥHBr�����л��е�������?? ���ջӷ����л�������ʯ����Һ������죬���ڵ��ܿ��а�������������dz��ɫ������Ag++Br���TAgBr��������Һ�ײ�����ɫ��״Һ�壻�屽�л������Ե��
��2��ȡ����Ӧ���Ƚ�ŨHNO3ע�������У�������ע��ŨH2SO4 �� ����ʱ���裻��Һ©��
���������⣺��1.���ٱ���Һ���������·�Ӧ�����屽���廯�⣬��Ӧ�Ļ�ѧ����ʽΪ�� ![]() �� ���Դ��ǣ�
�� ���Դ��ǣ� ![]() ��
��
�����ӷ����������л��ܼ���������C�����������廯���е���ͻӷ����л�����������ֹ���廯��ļ�����ɸ��ţ��廯������ˮ������������Ӻ������ӣ�������Һ�����ԣ���ʹʯ����ɫ�����ڵ��ܿ��а����������������е��������������ӷ�Ӧ���ɵ���ɫ�ij�������Ӧ�����ӷ���ʽΪ��Ag++Br��=AgBr����
���Դ��ǣ���ȥHBr�����л��е������������ջӷ����л���������ʯ����Һ������죬���ڵ��ܿ��а�������������dz��ɫ������Ag++Br���TAgBr����
�۱���Һ�巢��ȡ����Ӧ�����屽���廯�⣬�屽���ܶȴ���ˮ����ɫ����״Һ�壬�廯���ӷ�������ˮ������ϳ�������Һ�Σ�
���Դ��ǣ�����Һ�ײ�����ɫ��״Һ�壻�屽�л������Ե�ʣ�
��2.���ٱ������ᷢ��ȡ����Ӧ������������
���Դ��ǣ�ȡ����Ӧ��
��Ũ������Ũ�����Ϸų��������ȣ����ƻ������ע�������ǣ��Ƚ�Ũ����ע�������У�������ע��Ũ���ᣬ����ʱ�������ȴ��
���Դ��ǣ��Ƚ�ŨHNO3ע�������У�������ע��ŨH2SO4 �� ����ʱ���裻
������������״Һ�壬��ˮ�����ܣ����뻥�����ܵ�Һ̬����ȡ��Һ��������Ҫ�÷�Һ©����
���Դ��ǣ���Һ©����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��M��R��X��YΪԭ��������������Ķ���������Ԫ�أ�Z��һ�ֹ���Ԫ�أ�M��̬ԭ��L����p�����������s��������2����R��ͬ����Ԫ��������õĽ���Ԫ�أ�X��M�γɵ�һ�ֻ������������������Ҫ������Ⱦ�Z�Ļ�̬ԭ��4s��3d������������ش��������⣺
��1��R��̬ԭ�ӵĵ����Ų�ʽ�� �� X��Y�е縺�Խϴ��������Ԫ�ط��ţ���
��2��X���⻯��ķе��������������Ƶ�M���⻯���ԭ���� ��
��3��X��M�γɵ�XM3���ӵĿռ乹���� ��
��4��M��R���γɵ�һ�����ӻ�����R2M����ľ�����ͼ��ʾ����ͼ�к���������������������ӷ��ţ���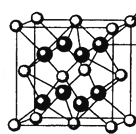
��5����ϡ�����У�Z����ۺ�����ļ��Σ���ɫ������M��һ���⻯�Z����ԭΪ+3�ۣ��÷�Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�����ʳ�����ڵ����³��ֶ���������ܷ�ʳ�ü����ͺ�������
A. ���ܣ���Ϊ�Ѿ�����
B. ���ܣ���Ϊ��������
C. ���ܣ���Ϊ����ˮ��
D. �ܣ���Ϊ��ֻ����֬��Ҫ�ɷ��ڵ����½ᾧ������������������̬�仯����δ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʰ����ϣ���һ���������������ɵĶ��ķ��ӹ���( )
A. 4�� B. 3�� C. 2�� D. 1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л�����
��1������֬�����������������������ʵ���ţ���ͬ����
��2�����ڷ��������� ��
��3�����ڱ���ͬϵ����� ��
��4������֬�������� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1.12g���ۼ���25mL 2mol/L��FeCl3��Һ�У���ַ�Ӧ�������ǣ� ��
A.������ʣ�࣬��Һ��dz��ɫ��Cl���������ֲ���
B.����Һ�е�����ɫKSCN��Һ�����Ժ�ɫ
C.Fe2+��Fe3+���ʵ���֮��Ϊ6��1
D.��������ͻ�ԭ��������ʵ���֮��Ϊ2��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Ũ�Ⱦ�Ϊ1 mol��L��1������4����Һ��
��H2SO4��Һ��NaHCO3��Һ��NH4Cl��Һ��NaOH��Һ
��1����4����ҺpH�ɴ�С��˳���� ��������ˮ�����H��Ũ����С���� ����������ţ�
��2�����и�����Ũ���ɴ�С��˳���� ��NaHCO3��ˮ��ƽ�ⳣ��Kh�� mol��L��1������֪̼��ĵ��볣��K1��4��10��7��K2��5.6��10��11��
��3��������ͨ��������������ʱ![]() ��ֵ ������������������С����������������
��ֵ ������������������С����������������
��4��������������Ϻ���Һǡ�ó����ԣ�����ǰ������� �����������������������С��������������֮һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ᣨHA�������Աȼ��ᣨHB�����������ʵ���Ũ�Ⱦ�Ϊ0.1mol/L��NaA��NaB�����Һ�У�����������ȷ���ǣ� ��
A. c(OH��)>c(HA)>c(HB)>c(H+) B. c(OH-)>c(A-)>c(B-)>c(H+)
C. c(OH-)>c(B-)>c(A-)>c(H+) D. c(OH-)>c(HB)>c(HA)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֲ�ͬ����CxHy��CaHb������ʲô������ϣ�ֻҪ������һ������ȫȼ��ʱ����O2������������ˮ���������䣬����������ȷ����(����)
A.CxHy��CaHb��������ԭ��ϵ��һ�����
B.������C2H4��C3H6�Ļ����
C.CxHy��CaHbһ����ͬ���칹��
D.CxHy��CaHb�����ʽ���Բ�ͬ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com