
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | ? | 2.1 | 2.3 | 3.0 | 0.8 |

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源:不详 题型:单选题
| A.在化工生产中应遵循“绿色化学”的思想 |
| B.控制实验条件可以改变化学反应的限度和速率 |
| C.在元素周期表的金属和非金属分界线附近寻找半导体材料 |
| D.根据元素周期律,由HClO4可以类推出氟元索也存在最高价氧化物的水化物HFO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
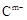 、
、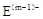 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题: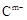 、
、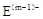 的还原性强弱顺序为:_________,(用离子符号表示)能证明其还原性强弱的离子方程式为________________________________。
的还原性强弱顺序为:_________,(用离子符号表示)能证明其还原性强弱的离子方程式为________________________________。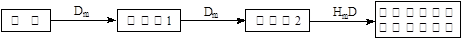
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第4 、5 、6周期的副族元素均为10个 |
| B.第三和第四周期的相同主族元素的原子序数一定相差18 |
| C.相同主族元素的价电子层排布一定相同 |
| D.元素周期表中第四周期第VA族的元素与第三周期IIA元素核电荷数相差13 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
族 周期 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | ⑦ | | ⑨ | ⑧ | |
 (2)②⑦⑨的最高价含氧酸的酸性由强到弱的顺序为________________________。
(2)②⑦⑨的最高价含氧酸的酸性由强到弱的顺序为________________________。 (3)①、④、⑤中的某些元素可形成既含离子键又含共价键的化合物,写出其中两种化合物的电子式: ___、 。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的化合物,写出其中两种化合物的电子式: ___、 。 (4)元素④的一种氢化物A在一定条件下分解为它的另一种氢化物B,写出A的结构式_______
(4)元素④的一种氢化物A在一定条件下分解为它的另一种氢化物B,写出A的结构式_______ 。
。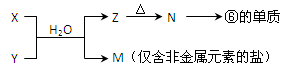
 X溶液与Y溶液反应的离子方程式为_____________________
X溶液与Y溶液反应的离子方程式为_____________________  N→⑥的单质的化学方程式为_____________ _
N→⑥的单质的化学方程式为_____________ _ 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素周期表中非金属元素都在短周期 |
| B.N、P、As得电子能力减弱。最高价氧化物对应水化物均可表示为H3YO4 |
| C.元素周期表中过渡元素只包括金属元素 |
| D.A一1zX、AzX、A+1zX在元素周期表中的位置、原子核外电子排布相同,但性质不同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com