
(每空2分,16分)生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水_________。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为________________ (不用写反应条件),原子利用率是_________ 。
(3)下列属于乙醇的同系物的是_____,属于乙醇的同分异构体的是_____。(选填编号)

(4)乙醇能够发生氧化反应:
① 46 g乙醇完全燃烧消耗__________mol氧气。
②乙醇在铜做催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为_____________。
③下列说法正确的是__________。(选填字母)
A.乙醇不能和酸性高锰酸钾溶液发生氧化还原反应
B.交警用橙色的酸性重铬酸钾溶液检查司机是否酒后驾车
C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了
D.陈年的酒很香是因为乙醇和乙醇被氧化生成的乙酸发生酯化反应生成了乙酸乙酯
(1)小
(2)CH2=CH2+H2O CH3CH2OH
CH3CH2OH
(3)D ,E
(4)① 3 ②2C2H5OH+O2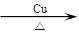 2CH3CHO+2H2O
③BCD
2CH3CHO+2H2O
③BCD
【解析】(1)考查乙醇的物理性质。
(2)乙烯和水发生加成反应生成乙醇,方程式为CH2=CH2+H2O CH3CH2OH。反应物完全转化为生成物,原子利用率是100%。
CH3CH2OH。反应物完全转化为生成物,原子利用率是100%。
(3)同系物是指结构相似,分子组成相差若干个CH2原子团的同一类物质。A属于酚类,B属于芳香醇,C和E是醚类,F是二元醇,所以只有甲醇和乙醇互为同系物。同分异构体是指分子式相同,而结构不同的化合物,乙醇的分子式为C2H6O,因此和甲醚互为同分异构体。
(4)乙醇燃烧的方程式为CH3CH2OH+3O2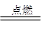 2CO2+3H2O,46 g乙醇是1mol,根据方程式可计算需要氧气3mol。乙醇含有唇羟基,可发生催化氧化,方程式为2C2H5OH+O2
2CO2+3H2O,46 g乙醇是1mol,根据方程式可计算需要氧气3mol。乙醇含有唇羟基,可发生催化氧化,方程式为2C2H5OH+O2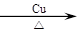 2CH3CHO+2H2O。醇羟基可以使酸性高锰酸钾溶液褪色,A不正确。BCD 均正确。
2CH3CHO+2H2O。醇羟基可以使酸性高锰酸钾溶液褪色,A不正确。BCD 均正确。


科目:高中化学 来源: 题型:
(每空2分,16分)生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水_________。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为________________ (不用写反应条件),原子利用率是_________ 。
(3)下列属于乙醇的同系物的是_____,属于乙醇的同分异构体的是_____。(选填编号)
(4)乙醇能够发生氧化反应:
① 46 g乙醇完全燃烧消耗__________mol氧气。
②乙醇在铜做催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为_____________。
③下列说法正确的是__________。(选填字母)
A.乙醇不能和酸性高锰酸钾溶液发生氧化还原反应
B.交警用橙色的酸性重铬酸钾溶液检查司机是否酒后驾车
C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了
D.陈年的酒很香是因为乙醇和乙醇被氧化生成的乙酸发生酯化反应生成了乙酸乙酯
查看答案和解析>>
科目:高中化学 来源:2011—2012学年度广东惠阳一中实验学校高二下学期3月月考化学试卷(带解析) 题型:填空题
(每空2分,16分)生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水_________。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为________________ (不用写反应条件),原子利用率是_________ 。
(3)下列属于乙醇的同系物的是_____,属于乙醇的同分异构体的是_____。(选填编号)
(4)乙醇能够发生氧化反应:
① 46 g乙醇完全燃烧消耗__________mol氧气。
②乙醇在铜做催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为_____________。
③下列说法正确的是__________。(选填字母)
| A.乙醇不能和酸性高锰酸钾溶液发生氧化还原反应 |
| B.交警用橙色的酸性重铬酸钾溶液检查司机是否酒后驾车 |
| C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了 |
| D.陈年的酒很香是因为乙醇和乙醇被氧化生成的乙酸发生酯化反应生成了乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源:2014届四川省高二10月月考化学试卷(解析版) 题型:填空题
(每空2分 共16分) 20世纪50年代科学家提出价层电子对互斥模型(简称VSEPR模型),用于预测简单分子立体结构。其要点可以概括为:
Ⅰ、用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤对电子),(n+m)称为价层电子对数。分子中的价层电子对总是互相排斥,均匀的分布在中心原子周围的空间;
Ⅱ、分子的立体构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤对电子; Ⅲ、分子中价层电子对之间的斥力主要顺序为: i、孤对电子之间的斥力>孤对电子对与共用电子对之间的斥力>共用电子对之间的斥力; ii、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力; iii、X原子得电子能力越弱,A-X形成的共用电子对之间的斥力越强; iv、其他。
请仔细阅读上述材料,回答下列问题:
(1)根据要点I可以画出AXnEm的VSEPR理想模型,请填写下表:
|
n+m |
2 |
|
|
VSEPR理想模型 |
|
正四面体 |
|
价层电子对之间的理想键角 |
|
109°28′ |
(2)请用VSEPR模型解释CO2为直线型分子的原因 。
(3) H2O分子的立体构型为: ,请你预测水分子中∠H-O-H的大小范围为 ,原因是 。
(4) SO2Cl2和SO2F2都属AX4E0型分子,S=O之间以双键结合,S-Cl、S-F之间以单键结合。请你预测 SO2Cl2和SO2F2分子的立体构型: 。
查看答案和解析>>
科目:高中化学 来源:2010年贵州省高三上学期第二次月考(理综)化学部分 题型:实验题
(每空2分,共14分)
(一)用碳酸钠粉末配制0.2000 mol·L-1Na2CO3溶液0.5L
(1)需选用的玻璃仪器或用品 (填字母编号)
B、0.5L 平底烧瓶 C、0.5L 容量瓶 D、0.5L圆底烧瓶 E、烧杯 F、试管 G、胶头滴管 H、量筒 I、托盘天平 J、药匙 M、滤纸 N、玻璃棒
(2)应称取 g 碳酸钠粉末来溶于水
(二)用0.2000 mol·L-1Na2CO3溶液标定未知浓度的盐酸
(1)把0.2000 mol·L-1Na2CO3溶液装入 (酸式,碱式)滴定管中。从此滴定管中放出20. 00mL0.2000 mol·L-1Na2CO3溶液入锥形瓶中,滴2至3滴甲基橙作指示剂,用未知浓度的盐酸来滴定0.2000 mol·L-1Na2CO3溶液,根据 判断滴定终点达到。
(2)终点达到时,用去盐酸16.00mL(三次的平均值),则盐酸c(HCl)=
(三)中和热的测定
用(二)实验中标定好浓度的盐酸50.0mL与0.55mol·L-1NaOH 50.0mL反应做中和热的测定实验。每次用量均一样,三次实验测得温度升高的平均值为3.41℃,则实验测得中和热△H= (混合后溶液的比热容C = 4.18J·℃-1·g-1),实验测得中和热比理论 (偏高,相等,偏低)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com