
【题目】氢气、一氧化碳、辛烷、甲烷燃烧的热化学方程式分别为
H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
CO(g)+![]() O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
C8H18(l)+![]() O2(g)=8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
O2(g)=8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是( )
A.H2B.COC.C8H18D.CH4
【答案】B
【解析】
由热化学方程式氢气、一氧化碳、辛烷、甲烷燃烧的热化学方程式分别为:
H2(g)+![]() O2(g)═H2O(l)△H=-285.8kJ/mol可知,1mol氢气燃烧放出的热量为285.8kJ,1mol氢气的质量为1mol×2g/mol=2g,故1g氢气燃烧放出的热量为:285.8kJ×
O2(g)═H2O(l)△H=-285.8kJ/mol可知,1mol氢气燃烧放出的热量为285.8kJ,1mol氢气的质量为1mol×2g/mol=2g,故1g氢气燃烧放出的热量为:285.8kJ×![]() =142.9kJ;
=142.9kJ;
由热化学方程式CO(g)+![]() O2(g)═CO2(g)△H=-283.0kJ/mol,可知,1molCO燃烧放出的热量为283kJ,1molCO的质量为1mol×28g/mol=28g,故1gCO燃烧放出的热量为:283kJ×
O2(g)═CO2(g)△H=-283.0kJ/mol,可知,1molCO燃烧放出的热量为283kJ,1molCO的质量为1mol×28g/mol=28g,故1gCO燃烧放出的热量为:283kJ×![]() =10.1kJ;
=10.1kJ;
由热化学方程式C8H18(l)+![]() O2(g)═8CO2(g)+9H2O(l)△H=-5518kJ/mol可知,1molC8H18燃烧放出的热量为5518kJ,1molC8H18的质量为1mol×114g/mol=114g,故1gC8H18燃烧放出的热量为:5818kJ×
O2(g)═8CO2(g)+9H2O(l)△H=-5518kJ/mol可知,1molC8H18燃烧放出的热量为5518kJ,1molC8H18的质量为1mol×114g/mol=114g,故1gC8H18燃烧放出的热量为:5818kJ×![]() =51kJ;
=51kJ;
由热化学方程式CH4 (g)+2O2(g)═CO2(g)+2H2O (l)△H=-890.3KJ/mol 可知,1molCH4燃烧放出的热量为890.3kJ,1molCH4的质量为1mol×16g/mol=16g,故1gCH4燃烧放出的热量为:890.3kJ×![]() =55.6kJ;
=55.6kJ;
则CO放出的热量最少,故答案为B。


科目:高中化学 来源: 题型:
【题目】香兰素是重要的香料之一,它可由丁香油酚经多步反应合成(见图)。有关上述两种化合物的说法不正确的是( )
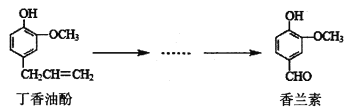
A.在丁香油酚分子中至少有12个原子共平面
B.常温下,1mol丁香油酚可与2molBr2反应
C.1moI香兰素最多能与4mol氢气发生加成反应
D.可用酸性KMnO4溶液检验丁香油酚中是否含有碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度、压强下,向密闭容器中投入一定量N2和H2,发生反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0。
2NH3(g) △H<0。
(1)反应开始阶段,V(正)_______(填“>”“<”或“=”)v(逆),随后v(正)逐渐______(填“增大”或“减小”,下同),v(逆)逐渐_________,反应达到平衡时,v(正)等于v(逆)。
(2)达到平衡后,若正反应速率用v(N2)表示,逆反应速率用v'(H2)表示,则v(N2)=_____v'(H2)。
(3)下列措施中能加快反应速率并提高氢气的转化率的是_____________(填字母)。
A.其他条件不变时,压缩容器体积 B.其他条件不变时,升高反应体系温度
C.使用合适的催化剂 D.保持容器体积不变,充入一定量的氮气
(4)实际生产中往往需要将温度控制在一个合适的范围,分析温度不宜过高也不宜过低的原因:_________________________________________________________。
(5)写出合成氨反应N2(g)+3H2(g)![]() 2NH3(g)的平衡常数表达式:____________________。升高温度时K值_________(填“增大”“减小”或“不变”)。
2NH3(g)的平衡常数表达式:____________________。升高温度时K值_________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解法处理酸性含铬废水(主要含有![]() )时,以铁板作阴、阳极,处理过程中存在反应
)时,以铁板作阴、阳极,处理过程中存在反应![]() +6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是 ( )
+6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是 ( )
A.阳极反应为Fe-2e-=Fe2+
B.电解过程中溶液c(H+)不会变化
C.处理过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有1 mol![]() 被还原
被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.按系统命名法,CH3CH(C2H5)CH2CH(CH3)2的命名为: 2-甲基-4-乙基戊烷
B.若两种二肽互为同分异构体,则二者的水解产物一定不相同
C.![]() 的单体是CH3-C≡C-CH3和CH2=CH-CN
的单体是CH3-C≡C-CH3和CH2=CH-CN
D.已知![]() 可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键
可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)A~G各物质间的关系如下图,其中B、D为气态单质。

请回答下列问题:
(1)物质C和E的名称分别为________________、__________________;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为_____________;
若只能在加热情况下进行,则反应物A应为_____________;
(3)反应②的化学方程式为_______________________________________;
(4)新配制的F溶液应加入_____________以防止其转化为G。检验G溶液中阳离子的常用试剂是_____________,实验现象为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸甲酯(属于酯类,代号M)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。测得其相对分子质量为162,分子中C、H、O原子个数比为5︰5︰1,且分子中只含有1个苯环,苯环上只有一个取代基。现测出M的核磁共振氢谱谱图有6个峰,其面积之比为1︰2︰2︰1︰1︰3。下列说法不正确的是
A.M的分子式为C10H10O2
B.1mol的M最多能被4molH2还原
C.肉桂酸能使溴水和酸性高锰酸钾溶液褪色
D.与M含有相同官能团,且苯环上氢的化学环境只有两种的同分异构体有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 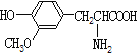 与
与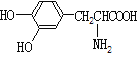 都是α-氨基酸且互为同系物
都是α-氨基酸且互为同系物
B. CH3CH=CHCH3分子中的四个碳原子在同一直线上
C. 按系统命名法,化合物按系统命名法,化合物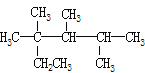 的名称是2,3,4-三甲基-2-乙基戊烷
的名称是2,3,4-三甲基-2-乙基戊烷
D. ![]() 的一溴代物和
的一溴代物和![]() 的一溴代物都有4种(不考虑立体异构)
的一溴代物都有4种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为确定一种从煤中提取的液态烃X的结构,对其进行探究。
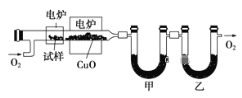
步骤一:这种碳氢化合物蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和固体氢氧化钠的吸收管完全吸收.2.12g有机物X的蒸气氧化产生7.04g二氧化碳和1.80g水;
步骤二:通过仪器分析得知X的相对分子质量为106;
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2∶3 (如图Ⅰ)
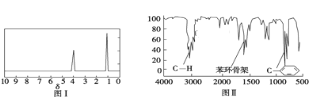
步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ,试回答:
(1)步骤二中的仪器分析方法称为___________。
(2)X的分子式为___________;(写出计算过程)X的结构简式为___________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com