
| A. | 升华 | B. | 蒸馏 | C. | 萃取 | D. | 过滤 |
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 如图是铜锌原电池的装置示意图.回答下列问题:
如图是铜锌原电池的装置示意图.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  可以进行酸碱中和滴定实验 | |
| B. | 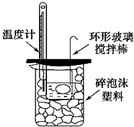 可以进行中和热的测定实验 | |
| C. | 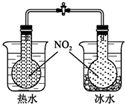 可验证温度对化学平衡的影响 | |
| D. |  比较Cu2+、Fe3+对H2O2分解速率的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数[φ(B)]的关系曲线,由曲线分析,下列判断正确的是( )
已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数[φ(B)]的关系曲线,由曲线分析,下列判断正确的是( )| A. | T1<T2,p1>p2,m+n>p,放热反应 | B. | T1>T2,p1<p2,m+n>p,吸热反应 | ||
| C. | T1<T2,p1>p2,m+n<p,放热反应 | D. | T1>T2,p1<p2,m+n<p,吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铝可以与氢氧化钠溶液反应 | |
| B. | 向硅酸钠溶液中滴加适量稀盐酸,有透明的凝胶形成 | |
| C. | 氯气通入石蕊中先变红后褪色 | |
| D. | 向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、SO42-、Cu2+、Cl- | B. | Fe2+、NO3-、Na+、Al3+ | ||
| C. | Mg2+、H+、Cl-、NO3- | D. | Ag+、K+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1780 | B. | 1220 | C. | -1220 | D. | -1780 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com