
下列离子方程式改写成化学方程式正确的是
A.Cu2+ + 2OH- = Cu(OH)2↓ CuSO4+Ba(OH)2= Cu(OH)2↓+ Ba2SO4↓
B.CO32- + 2H+ = CO2↑+ H2O NaHCO3 + HCl =NaCl+ CO2↑+ H2O
C.H+ +OH- = H2O NaOH+HNO3=NaNO3+H2O
D.SO42-+Ba2+=BaSO4↓ BaCl2+H2SO4=BaSO4↓+2HCl
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案科目:高中化学 来源:2014-2015广东省高二上学期期中联考化学(文)试卷(解析版) 题型:?????
蓝宝石的主要成分为ⅢA族元素的氧化物,该氧化物为
A.Al2O3 B.SiO2
C.Fe2O3 D.MgO
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省高二上学期期中联考化学(理)试卷(解析版) 题型:填空题
(12分)PNA是一种具有良好的热稳定性、耐腐蚀性和抗水性的高分子化合物,常用作塑化剂,其合成路线如下图所示:

已知:①R1CH=CHR2 R1COOH + R2COOH (R1、R2代表烃基)
R1COOH + R2COOH (R1、R2代表烃基)
②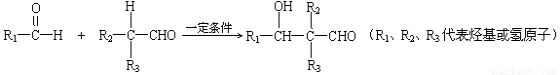
请回答:
(1)E→F的反应类型是 。
(2)C含有的官能团名称是 。
(3)A分子中只有一个氯原子,A→B的化学方程式是 。(注明反应条件)
(4)D能发生银镜反应,且分子中有支链,D的结构简式是 。
(5)E的结构简式是 。
(6)C与F在一定条件下生成增塑剂PNA的反应的化学方程式是: 。(不用注明反应条件)
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省高二上学期期中联考化学(理)试卷(解析版) 题型:选择题
下列烷烃的命名正确的是
A.2,4-二乙基戊烷 B.4-甲基-3-乙基已烷
C.2-甲基-3-丙基戊烷 D.2,3,3-三甲基戊烷
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市高一上学期10月月考化学试卷(解析版) 题型:填空题
(16分)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓) 2KCl + 2MnCl2 + 5Cl2↑ +8H2O
(1)用单线桥法标出电子转移的方向和数目。
(2)该反应中的氧化剂与还原剂物质的量之比是 。
(3)KMnO4的氧化性比Cl2的氧化性 (选填“强”或“弱”)。
(4)如反应中转移了2mol电子,则产生的Cl2在标准状况下体积为 L。
(5)某同学欲用KMnO4固体配制100 mL0.5mol.L-1的溶液。回答下列问题:
①配制KMnO4溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、 、 。
②应用托盘天平称取KMnO4固体 g。
③不规范的实验操作会导致实验结果的误差。分析下列操作对实验结果的影响偏小的是(请填序号) 。
A.加水定容时俯视刻度线
B.容量瓶内壁附有水珠而未干燥处理
C.颠倒摇匀后发现凹液面低于刻度线又加水补上
D.在溶解过程中有少量液体溅出烧杯外
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市高一上学期10月月考化学试卷(解析版) 题型:选择题
甲、乙两烧杯中各盛有100mL 3mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中加入等质量的铝粉,反应结束后生成气体的体积比为甲:乙=1:2,则加入铝粉的质量为
A.1.8g B.3.6g C.2.7g D.5.4g
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市高一上学期10月月考化学试卷(解析版) 题型:选择题
下列例子方程式中,错误的是
A.向AlCl3中加入过量氨水: Al3++3NH3·H2O== Al(OH)3↓+3NH4+
B.硫酸氢钠溶液中加入足量的烧碱溶液:H++OH-=== H2O
C.过氧化钠加入水: 2Na2O2+2H2O==4OH-+O2↑+4Na+
D.金属铝溶于氢氧化钠溶液:2Al+2OH-==2AlO2-+H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高三上学期期末考试化学试卷(解析版) 题型:实验题
(15分)焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5

(1)装置Ⅰ中产生气体的化学方程式为 。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 。
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为 (填序号)。

实验二 葡萄酒中抗氧化剂残留量的测定
(4)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测得结果 (填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市七校高三上学期期末联考理综化学试卷 (解析版) 题型:推断题
(共14分)已知化合物A与B、丙与丁的组成元素分别相同,且四种物质中都含有同一种元素。A与B在常温下均呈液态。D与F都为固体单质,且D、 F与甲的浓溶液在常温下都会出现钝化现象,加热时有大量气体产生。(相关转化及部分反应条件和生成物未标出)。

(1)A的结构式 , E与F的反应是 (填反应名称),写出2种该反应在工业生产中的用途: 、 。
(2)若反应①除生成甲外,还生成丙,写出过量D与甲的稀溶液反应的离子方程式:
(3)若A与丙可以化合生成甲;D与甲的浓溶液加热条件下可以生成三种化合物乙、丙、B,写出下列化学方程式②: ③:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com