
比较下列各组热化学方程式中ΔH的大小关系。
(1)S(s)+O2(g)===SO2(g) ΔH1
S(g)+O2(g)===SO2(g) ΔH2
ΔH1______ΔH2
(2)CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1
CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH2
ΔH1______ΔH2
(3)煤作为燃料有两种途径:
途径1——直接燃烧
C(s)+O2(g)===CO2(g) ΔH1<0
途径2——先制水煤气
C(s)+H2O(g)===CO(g)+H2(g) ΔH2>0
再燃烧水煤气:
2CO(g)+O2(g)===2CO2(g) ΔH3<0
2H2(g)+O2(g)===2H2O(g) ΔH4<0
ΔH1、ΔH2、ΔH3、ΔH4的关系式是______________________________________。
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:
2012年“六·五”世界环境日主题:“绿色消费,你行动了吗?”旨在强调绿色消费的理念,选择绿色产品。以下叙述与此理念不相符的是( )
①在食盐中加入适量碘酸钾防治碘缺乏症
②用工业酒精兑制饮用酒以降低成本
③用活性炭来脱色以制白糖
④加工香肠时任意加入亚硝酸钠以保持肉类新鲜
⑤做馒头时加入适量纯碱或碳酸氢钠使馒头松软
A.②和④ B.①和③ C.③和⑤ D.②和⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
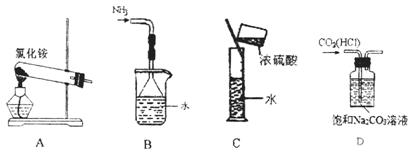
下列实验装置、选用的试剂或实验操作中,都正确的是
A.实验室用装置A制取氨气
B.用B装置吸收氨气,并防止倒吸
C.用C装置稀释浓硫酸
D.用D装置除去CO2中的HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
根据以下3个热化学方程式
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l) ΔH=-Q1 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(l) ΔH=-Q2 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(g) ΔH=-Q3kJ·mol-1
判断Q1、Q2、Q3三者关系正确的是( )
A.Q1>Q2>Q3 B.Q1>Q3>Q2 C.Q3>Q2>Q1 D.Q2>Q1>Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学反应热问题的说法正确的是( )
A.放热反应发生时不必加热
B.化学反应一定有能量变化
C.一般地说,吸热反应加热后才能发生
D.化学反应的热效应数值与参加反应的物质的多少无关
查看答案和解析>>
科目:高中化学 来源: 题型:
煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:
a.C(s)+O2(g)===CO2(g) ΔH=E1①
b.C(s)+H2O(g)===CO(g)+H2(g) ΔH=E2②
H2(g)+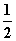 O2(g)===H2O(g) ΔH=E3③
O2(g)===H2O(g) ΔH=E3③
CO(g)+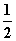 O2(g)===CO2(g) ΔH=E4④
O2(g)===CO2(g) ΔH=E4④
回答:
(1)上述四个热化学方程式中的哪些反应ΔH<0?
________________________________________________________________________。
(2)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是( )
A.a比b多 B.a比b少 C.a与b在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为________________________
________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,我国拥有的完全自主产权的氢氧燃料电池车已在北京奥运会期间为运动员提供了服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
A.正极反应式为O2+2H2O+4e-—→4OH-
B.工作一段时间后,电解液中KOH的物质的量不变
C.该燃料电池的总反应方程式为2H2+O2===2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
温度为T时,向2.0 L 恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)====PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
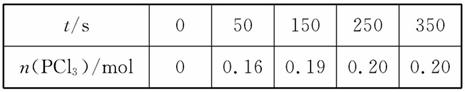
下列说法正确的是( )
A.反应在前50 s的平均速率
v(PCl3)=0.003 2 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L-1,则反应的ΔH<0
C.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol  PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3 的转化率小于80%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com