
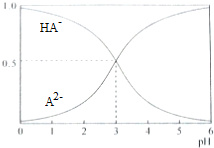
 室温下,1mol/L的某二元酸H2A溶液中,可能存在的含A粒子(H2A,HA-,A2-)的物质的量分数(x)随pH变化的关系下图所示,下列说法正确的是( )
室温下,1mol/L的某二元酸H2A溶液中,可能存在的含A粒子(H2A,HA-,A2-)的物质的量分数(x)随pH变化的关系下图所示,下列说法正确的是( )| A. | H2A的电离方程式为H2A?H+HA- | |
| B. | 将pH=2的NaHA和Na2A混合溶液中加水稀释10倍,溶液的pH=3 | |
| C. | 将相同物质的量的NaHA和Na2A固体溶于水所得混合溶液的pH一定为3 | |
| D. | Na2A溶液存在:c(0H-)=c(H+)+c(HA-) |
分析 A、二元酸H2A溶液中不存在H2A分子,说明第一步完全电离,二元酸H2A的电离方程式为:H2A=H++HA- HA-?H++A2-;
B、加水稀释促进HA-的电离;
C、不知道HA-的电离程度与A2-的水解程度哪个更大;
D、根据质子守恒分析.
解答 解:A、二元酸H2A溶液中不存在其分子,说明第一步完全电离,二元酸H2A的电离方程式为:H2A=H++HA-,HA-?H++A2-,故A错误;
B、将pH=2的NaHA和Na2A混合溶液中加水稀释10倍,加水稀释促进HA-的电离,H+的物质的量增大,所以pH变化小于1个单位,则溶液的pH<3,故B错误;
C、不知道HA-的电离程度与A2-的水解程度哪个更大,将相同物质的量的NaHA和Na2A固体溶于水所得混合溶液,其溶液的pH不一定是3,故C错误;
D、Na2A溶液存在质子守恒,即水电离的氢离子总浓度等于水电离的氢氧根离子的总浓度,即c(0H-)=c(H+)+c(HA-),故D正确;
故选D.
点评 本题考查了据图象分析二元酸的电离特点,关键是从图象分析出第一步完全电离,题目难度中等,侧重于考查学生的分析能力和计算能力.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于2SO2(g)+O2(g)?2SO3(g)△H=-QkJ/mol(Q>0),若向一密闭容器中加入1molSO2和0.5molO2充分反应后,放出的热量为0.5QkJ | |
| B. | 热化学方程式中的化学计量数表示相应物质的物质的量,不能用分数表示 | |
| C. | 需要加热才能发生的反应不一定是吸热反应 | |
| D. | 小苏打在水中的电离方程式:NaHCO3═Na++H++CO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X是非金属元素 | |
| B. | X形成含氧酸钾盐化学式可能为KXO2、KXO3或KXO4 | |
| C. | 由X形成的含氧酸均为强酸 | |
| D. | X不可能为第一周期元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅胶多孔,常用作食品干燥剂和催化剂的载体 | |
| B. | 用灼烧和闻气味的方法区别棉织物和纯毛织物 | |
| C. | 用SO2漂白过的草帽缏日久会变色 | |
| D. | 氯气处理饮用水,在夏季的杀菌效果比在冬季好 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
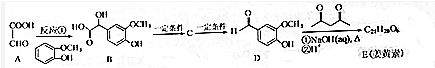
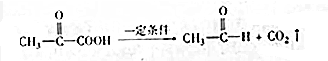


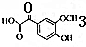
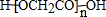
 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化学反应N2(g)+3H2(g)=2NH3(g)的能量变化如图所示,请回答下列问题:
化学反应N2(g)+3H2(g)=2NH3(g)的能量变化如图所示,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
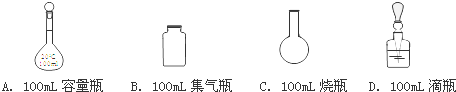
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com