
| A. | 黑色沉淀完全转化为白色沉淀 | B. | 既有氯化银也有硫化银 | ||
| C. | 只产生黑色硫化银沉淀 | D. | 只有氯化银白色沉淀 |
分析 由Ksp(AgCl)=1.8×10-10、Ksp(Ag2S)=6.3×10-50可知,Ag2S更难溶,则Ag2S不能转化为AgCl,以此来解答.
解答 解:盛有0.1mol/L AgNO3溶液的试管中,滴加0.1mol/L Na2S溶液直至沉淀完全,Ag+完全转化为Ag2S黑色沉淀,由Ksp(AgCl)=1.8×10-10、Ksp(Ag2S)=6.3×10-50可知,Ag2S更难溶,向其中滴加足量NaCl溶液,则Ag2S不能转化为AgCl,即不能由黑色沉淀转化为白色沉淀,
故选C.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握银离子完全沉淀及沉淀转化为解答的关键,侧重分析与应用能力的考查,注意沉淀生成与沉淀转化的判断,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
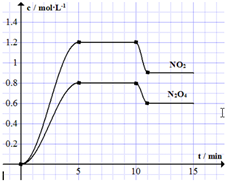
| A. | 前5min反应的平均速率v(NO)=0.24mol•(L•min)-1 | |
| B. | T℃时反应①的化学平衡常数K=0.36 | |
| C. | 10min时改变反应条件可能是降低温度 | |
| D. | 若起始时向该容器中充入1.6mol NO2和4.0mol N2O4,T℃达到平衡时,NO2的物质的量浓度与图中5~10min的不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
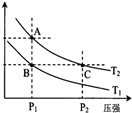 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 相同温度下,同浓度的溶液的pH:CH3COONa>Na2CO3>NaHCO3>NaClO | |
| B. | 同温同浓度的三种溶液:①(NH4)2SO4②(NH4)2CO3③(NH4)2FeSO4 c (NH4+)大小:②>①>③ | |
| C. | 室温时pH=8的NaOH溶液与pH=8的氨水等体积混合pH等于8 | |
| D. | 向1mL0.1mol/L AgNO3溶液中滴加3~5滴0.1mol/L NaCl溶液,产生白色沉淀,再滴入KI溶液,沉淀变成黄色,由此推出:Ksp(AgI)<Ksp(AgCl) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com