
A、氢气、CO合成甲醇:2H2+CO
| ||
B、烯烃与水煤气发生反应:RCH=CH2+CO+H2
| ||
| C、CH4与Cl2反应制取CCl4 | ||
| D、氯乙烯合成聚氯乙烯 |


科目:高中化学 来源: 题型:
| H2O/H- |
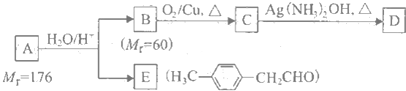
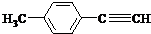 )的一条路线如下:
)的一条路线如下: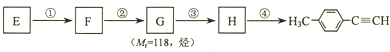
查看答案和解析>>
科目:高中化学 来源: 题型:
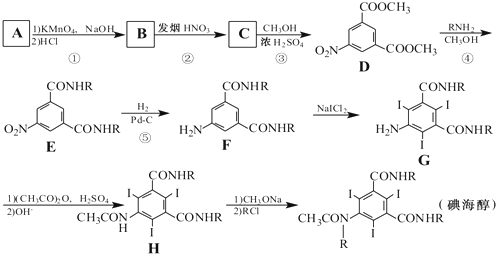
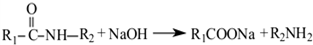
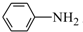 呈弱碱性,易被氧化请写出以和(CH3CO)2O为原料制备染料中间体
呈弱碱性,易被氧化请写出以和(CH3CO)2O为原料制备染料中间体 的合成路线流程图(无机试剂任用)
的合成路线流程图(无机试剂任用)| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.00 | 20.30 |
| 第二次 | 25.00 | 0.00 | 20.20 |
| 第三次 | 25.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、合成氨生产过程中将NH3液化分离,会降低反应速率,可提高N2、H2的转化率 |
| B、从海水中提镁过程中,电解熔融MgO可制备Mg |
| C、电解精炼铜时,同一时间内阳极溶解固体的质量比阴极析出固体的质量小 |
| D、电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X中一定不存在FeO |
| B、不容物Y中一定含有FeO和CuO |
| C、Z溶液中一定存在K2CO3 |
| D、Y中一定存在MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
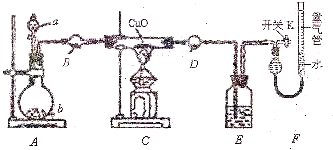
| 实验数据1 | 实验数据2 | 实验数据3 | |
| 甲小组 | 反应前氧化铜的质量为m1g | 氧化铜反应后剩余固体的质量为m2g | 生成氮气在标准状况下的体积为V1L |
| 乙小组 | 洗气前装置D的质量为m3g | 洗气后装置D的质量为m4g | 生成氮气在标准状况下的体积为V2L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用过滤的方法除去食盐中的泥沙 |
| B、用分液的方法分离汽油和水 |
| C、用结晶的方法分离氯化钠和硝酸钾 |
| D、用加热的方法除去碳酸氢钠中混有的碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com