
| A. | K+、Ca2+、Cl-、CO${\;}_{3}^{2-}$ | B. | Na+、I-、Cl-、OH- | ||
| C. | NH${\;}_{4}^{+}$、NO${\;}_{3}^{-}$、K+、OH- | D. | Na+、Al3+、SO${\;}_{4}^{2-}$、HCO${\;}_{3}^{-}$ |
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:A>B>C>D | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:D>C>B>A | D. | 金属性:B>A,非金属性:D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
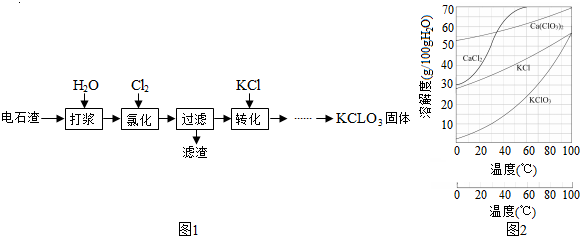
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 已知某燃料含有碳、氢、氧三种元素.为了测定该燃料的结构,现将1.04g燃料放人足量的氧气中充分燃烧,经测定消耗氧气1.568L(已转换为标准状况),并使产生的气体全部通人如图所示的装置,得到如表所示的实验数据(假设产生的气体被完全吸收,且没有空气进人该装置).
已知某燃料含有碳、氢、氧三种元素.为了测定该燃料的结构,现将1.04g燃料放人足量的氧气中充分燃烧,经测定消耗氧气1.568L(已转换为标准状况),并使产生的气体全部通人如图所示的装置,得到如表所示的实验数据(假设产生的气体被完全吸收,且没有空气进人该装置). | 实验前 | 实验后 | |
| A装置的质量 | 101.1g | 102.18g |
| B装置的质量 | 312.0g | 314.2g |
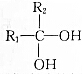 →
→ +H2O
+H2O查看答案和解析>>
科目:高中化学 来源: 题型:填空题
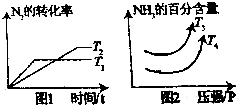 硝酸工业是国民经济的命脉产业,工业制硝酸通常是如下过程
硝酸工业是国民经济的命脉产业,工业制硝酸通常是如下过程查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com