
A��J�ֱ��ʾ��ѧ��ѧ�г�����һ�����ʣ�����֮�����ϵ����ͼ��ʾ�����ַ�Ӧ�������û���г���������֪GΪ����Ԫ�صĹ�̬����� A��B��C��D��E��F���������о���ͬһ��Ԫ�ء�
����д���пհף�
��1��A��B��C��D��E��F��������������ͬһ��Ԫ�������ڱ���λ���� ��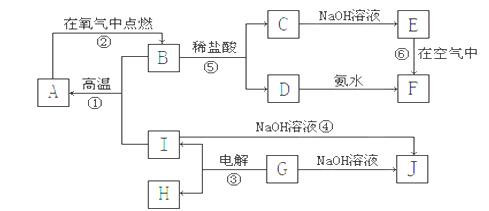
��2������C��Һ�������ӷ����ǣ�д�������������ۣ�
��
��3��д����Ӧ�ٻ�ѧ����ʽ�� ��
��4��д����Ӧ�����ӷ���ʽ�� ��
��5��д����Ӧ��ѧ����ʽ�� ��
��6��д����Ӧ�������ĵ缫��Ӧʽ�� ��
��7���������仯�Ƕȿ�����Ӧ�٢ڢ��У����ڡ�H��0�ķ�Ӧ�� ������ţ���
 ���ɶ��ȫ���ƿؾ�ϵ�д�
���ɶ��ȫ���ƿؾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Դ���������Ϊ��Լ������ᾭ�÷�չ��ƿ����Խ��Խ��Ĺ��ҿ�ʼʵ�С�����ƻ���������̫������Դ��Ѱ�÷�չ���¶�����

��1��̫������ˮ���г�ʹ��һ�����������Ͻ������Ϊ���ռ���̫��������Ϳ�㣬д����̬��ԭ�ӵ���Χ�����Ų�ʽ__________����λ�����ڱ�____________����
��2�� ����ϩ���������ھ������õĹ�����ܣ���̫���ܵ�ص�Ӧ���Ͼ��зdz�������ǰ;������ϩ��C60���Ľṹ����ͼ��������̼ԭ�ӹ�����ӻ�����Ϊ________��1 mol C60�����ЦҼ�����ĿΪ____________����
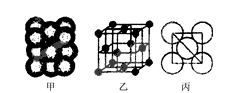
��3��Cu���ʾ�����ԭ�ӵĶѻ���ʽ����ͼ����ʾ���侧����������ͼ����ʾ��ԭ��֮���λ�ù�ϵ��ƽ��ͼ����ͼ����ʾ��������Cuԭ�ӵ���λ��Ϊ____________��һ��������Cuԭ�ӵ���ĿΪ________��
��4��Fe��CO��5�����³�Һ̬���۵�Ϊ��20��5 �棬�е�Ϊ103 �棬�����ڷǼ����ܼ����ݴ˿��ж�Fe��CO��5��������________��������ͣ���Fe��CO��5���������壮��λ���ֱ���________��________��
��5������˵����ȷ����________��
A����һ�����ܴ�С��S��P��Si
B���縺��˳��C��N��O��F
C����Ϊ������CaO��KCl�ߣ�����KCl��CaO�۵��
D��SO2��CO2�Ļ�ѧ�������ƣ����ӽṹҲ����ֱ���ͣ���ͬ������SO2���ܽ�ȸ���
E�����Ӿ����У����ۼ�����Խ�÷��Ӿ�����ۣ��е�Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��Һ����Fe3����Mg2����Fe2����Al3�����������ӣ��������м������������������Һ�� ������ټ�����������ᣬ��Һ�д������ٵ���������
A��Fe3�� B��Mg2�� C��Fe2�� D��Al3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
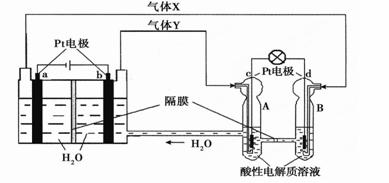
�ռ�ʵ���ҡ��칬һ�š��Ĺ���ϵͳ������������ȼ�ϵ�أ�RFC����RFC��һ�ֽ�ˮ��⼼��������ȼ�ϵ�ؼ������ϵĿɳ�ŵ�ء���ͼΪRFC����ԭ��ʾ��ͼ���й�˵����ȷ����( )
A. ����0.1mol����ת��ʱ��a������1.12L O2����״���£�
B. b���Ϸ����ĵ缫��Ӧ�ǣ�4H2O + 4e- = 2H2��+ 4OH-
C. d���Ϸ����ĵ缫��Ӧ�ǣ�O2 + 4H+ + 4e- = 2H2O
D. c���Ͻ��л�ԭ��Ӧ��B�е�H+����ͨ����Ĥ����A
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
NA��ʾ�����ӵ�����������˵����ȷ���ǣ� ��
A��1 mol Na������O2��Ӧ����Na2O��Na2O2��ʧȥNA������
B��1 mol Al�ֱ�������������ŨHNO3��ϡHNO3�У���Ӧ��ת�Ƶĵ��Ӿ�Ϊ3NA
C����5.6 g���ֱ������������ᡢ������Ӧ������ת��������Ϊ0.3NA
D��24 gþ�������������NaOH��Һ��Ӧת�Ƶĵ�����Ŀ��Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ֪ʶ�����������������Ź㷺��Ӧ�á�����˵��������ȷ���ǣ�
A����ֲ��ոѡ��������������������һ��������Դ
B���ֻ����õ�����ӵ�����ڶ��ε��
C����ˮ�����ܽ����ˮ��ӦΣ������ˮ�мӾ�ˮ����������ʹ��ˮ����
D�����ƿ���ȼ�ϵ������������Ч���ͻ�����β����Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й�ʵ���˵����ȷ���ǣ�
A���к͵ζ�ʱ���ô�����Һ��ϴ��ƿ
B��ʹ��pH��ֽ�ⶨ��ҺpHʱ����ʪ��������Һ��pHһ��ƫС
C������ʽ�ζ�����ȡ12.00 mL���������Һ
D�������Ƶ�����������Һ������һ���������ۺ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����100mL 1mol/L������п���ķ�Ӧ����ȡ���д�ʩ��ʹ��Ӧ���ʼӿ����
�������¶ȣ��ڸ���100mL 3mol/L����۶���300mL 1mol/L������õ���п�۴���п�����ݵ�������CuSO4��Һ
A���٢ڢܢ� B���٢ۢܢ� C���٢ڢۢ� D���٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ط�Ӧ�����ӷ���ʽ��д��ȷ���ǣ�������
A��4molFe ��5molCl2�е�ȼ��Ӧ��5Cl2+4Fe=2FeCl2+2FeCl3
B���Ȼ�����Һ��ͨ�����⣺2Fe3++H2S=2Fe2++S��+2H+
C��NH4Al��SO4��2��Һ�м���Ba��OH��2��ҺʹSO42-��ȫ������Al3++2SO42-+2Ba2++4OH-�TAlO2-+2BaSO4��+2H2O
D��NaHCO3��Һ�м��������Ba��OH��2��Һ��
2HCO3-+Ba2++2OH-�TBaCO3��+2H2O+CO32-
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com