
【题目】下列实验操作说法正确的是( )
选项 | 实验操作 | 现象与结论(或装置用途) |
A | 某溶液加入浓NaOH溶液加热,在试管口放一片湿润的红色石蕊试纸 | 试纸变蓝,说明NH3是碱 |
B |
| 可以用于比较Fe3+、I2、Cl2的氧化性强弱 |
C | 2mL 2% CuSO4中加4~6滴2% NaOH溶液,振荡后加入0.5mL X溶液,加热煮沸 | 未出现砖红色沉淀,说明X不含有醛基 |
D |
| 用于吸收HCl气体能防倒吸 |
A.A
B.B
C.C
D.D
【答案】B
【解析】解:A.氨气不能电离出氢氧根离子,所以不是碱,一水合氨电离出的阴离子全部是氢氧根离子,所以一水合氨是碱,故A错误; B.氯气先和碘离子反应生成碘,碘易溶于四氯化碳而使四氯化碳呈紫色,后和亚铁离子反应生成铁离子,铁离子易溶于水中,铁离子呈黄色,所以可以根据哪层液体先变色确定离子反应先后顺序,从而判断氧化性强弱,故B正确;
C.醛基和新制氢氧化铜悬浊液必须在碱性、加热条件下反应,该实验中NaOH不足量,所以不能实现实验目的,故C错误;
D.有缓冲作用的装置能防止倒吸,HCl极易溶于水,不溶于苯,所以没有缓冲作用,不能防止倒吸,可以将苯换为四氯化碳,故D错误;
故选B.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】室温时,向一密闭容器中充入2 mol SO2和2 mol O2 , 在一定条件下发生反应:2SO2+O2 ![]() 2SO3 , 该反应达到最大限度时,下列说法正确的是( )
2SO3 , 该反应达到最大限度时,下列说法正确的是( )
A.正反应的速率为零
B.SO2完全转化为SO3
C.SO3的物质的量浓度不再变化
D.SO2、O2和SO3的物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝土矿的主要成分是Al2O3、Fe2O3、SiO2等,从铝土矿冶炼Al2O3的流程如图: 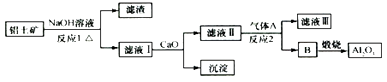
下列说法正确的是( )
A.气体A一定为HCl
B.滤液Ⅰ中溶质可能含NaAlO2
C.沉淀的主要成分不是硅酸钙
D.反应1、反应2均是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.1 mol OD﹣离子含有的质子、中子数均为10NA
B.标准状况下,4.48 L己烷含有的分子数为0.2NA
C.标准状况下,6.72LNO2与水反应消耗的氧化剂分子数为0.2NA
D.丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】瑞典ASES公司设计的曾用于驱动潜艇的液氨﹣液氧燃料电池示意图如图所示,下列有关说法正确的是( ) 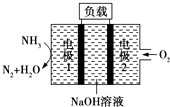
A.电池工作时,Na+向电极1移动
B.电池工作一段时间后停止,溶液PH值比开始时明显减小
C.电极1发生的电极反应为2NH3+6OH﹣﹣6e﹣═N2↑+6H2O
D.用该电池做电源电解精炼铜,理论上每消耗0.2 mol NH3的同时阳极会得到19.2g纯铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:2CH3OH(g)═CH3OCH3(g)+H2O(g)
下列说法正确的是( )
容器 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
A.该反应的正方应为吸热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH30.15mol和H2O 0.10mol,则反应将向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 ![]() 为阿伏加德罗常数的值。下列说法正确的是( )
为阿伏加德罗常数的值。下列说法正确的是( )
A.0.1 mol 的 ![]() 中,含有
中,含有 ![]() 个中子
个中子
B.pH=1的H3PO4溶液中,含有 ![]() 个
个 ![]()
C.2.24L(标准状况)苯在O2中完全燃烧,得到 ![]() 个CO2分子
个CO2分子
D.密闭容器中1 mol PCl3与1 mol Cl2反应制备 PCl5(g),增加 ![]() 个P-Cl键
个P-Cl键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com