
| A. | “类钫”在化合物中呈+1价 | |
| B. | 类钫具有放射性 | |
| C. | 单质与水反应较为缓慢 | |
| D. | 类钫最高价氧化物对应的水化物是强碱 |
分析 119号“类钫”是第8周期ⅠA族的元素,为碱金属元素,同主族最高正化合价相同,同主族向上而下金属性逐渐增强,单质与水的反应比较剧烈,其最高价氧化物对应水合物为一定为强碱;结合原子序数从84号开始的元素均为放射性元素进行判断.
解答 解:119号“类钫”是第8周期ⅠA族的元素,为碱金属元素,
A.碱金属最外层电子数都为1,根据主族元素最外层电子数等于最高正化合价可知,“类钫”在化合物中呈+1价,故A正确;
B.原子序数从84号开始的元素均为放射性元素,而“类钫”的原子序数为119,具有放射性,故B正确;
C.碱金属从上到下,金属性逐渐增强,则其单质与水反应比较剧烈,故C错误;
D.碱金属从上到下,原子序数越大,金属性越强,则类钫最高价氧化物对应的水化物是强碱,故D正确;
故选C.
点评 本题主要考查元素周期律的内容及应用,题目难度不大,明确原子结构与元素周期律的内容为解答关键,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
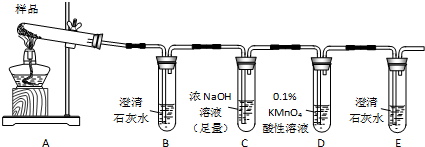
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 34 | B. | 40 | C. | 46 | D. | 114 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{22.4}$mol/L | B. | $\frac{1}{44.8}$mol/L | C. | $\frac{1}{33.6}$mol/L | D. | 无法计算 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com