
 HCOOH(l)��CH3OH(l)����H>0��ijС��ͨ��ʵ���о��÷�Ӧ(��Ӧ����������仯���Բ���)����Ӧ��ϵ�и���ֵ���ʼ�����±���
HCOOH(l)��CH3OH(l)����H>0��ijС��ͨ��ʵ���о��÷�Ӧ(��Ӧ����������仯���Բ���)����Ӧ��ϵ�и���ֵ���ʼ�����±���| ��� | HCOOCH3 | H2O | HCOOH | CH3OH |
| ���ʵ���/ mol | 1.00 | 1.99 | 0.01 | 0.52 |
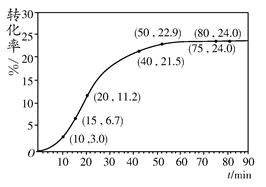
| ��Ӧʱ�� ��Χ/min | 0��5 | 10��15 | 20��25 | 30��35 | 40��45 | 50��55 | 75��80 |
| ƽ����Ӧ���� /(10��3 mol��min��1 | 1.9 | 7.4 | 7.8 | 4.4 | 1.6 | 0.8 | 0.0 |




| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO2(g)��H2(g)����Ӧ�����вⶨ�IJ������ݼ��±�(����t2��t1)������˵����ȷ����
CO2(g)��H2(g)����Ӧ�����вⶨ�IJ������ݼ��±�(����t2��t1)������˵����ȷ����| ��Ӧʱ��/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | | 0.20 |
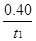 mol��L��1��min��1
mol��L��1��min��1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 cC(s)+dD,����Ӧ���е���t minʱ,���A������n mol,B������n/2 mol,C������3n/2 mol,D������n mol����ʱ��Ӧ�ﵽƽ�⡣
cC(s)+dD,����Ӧ���е���t minʱ,���A������n mol,B������n/2 mol,C������3n/2 mol,D������n mol����ʱ��Ӧ�ﵽƽ�⡣�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
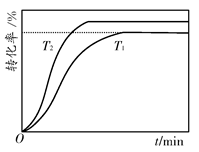
 2B(g)����H��-a kJ��mol��1������B�����ʵ���Ũ����ʱ��仯��ͼ��ʾ��
2B(g)����H��-a kJ��mol��1������B�����ʵ���Ũ����ʱ��仯��ͼ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 AB��˵�������°�����������з�Ӧ��
AB��˵�������°�����������з�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 yC(g)����H��0����һ�������£�������A��C�����ʵ���Ũ����ʱ��仯��������ͼ��ʾ����ش��������⣺
yC(g)����H��0����һ�������£�������A��C�����ʵ���Ũ����ʱ��仯��������ͼ��ʾ����ش��������⣺
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 3C��4D��Ӧ�У���ʾ�÷�Ӧ����������(����)��
3C��4D��Ӧ�У���ʾ�÷�Ӧ����������(����)���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com