
| A£® | ³£ĪĀĻĀ£®NH4ClČÜŅŗ¼ÓĖ®Ļ”ŹĶ£¬$\frac{c£ØN{H}_{3•}{H}_{2}O£©•c£Ø{H}^{+}£©}{c£ØN{{H}_{4}}^{+}£©}$Ōö“ó | |
| B£® | 0.1mol/LNa2CO3ČÜŅŗ¼ÓČČŗó£¬ČÜŅŗµÄpH¼õŠ” | |
| C£® | ŹŅĪĀĻĀĻ”ŹĶO£®lmol/LCH3COOHČÜŅŗ£¬ČÜŅŗµÄµ¼µēÄÜĮ¦¼õČõ£¬Ņņ“ĖČÜŅŗÖŠĖłÓŠĄė×ÓÅØ¶Č¾ł¼õŠ” | |
| D£® | Ļņ·ŠĖ®ÖŠµĪ¼ÓFeCl3±„ŗĶČÜŅŗÖʱøFe£ØOH£©3½ŗĢåµÄŌĄķŹĒ¼ÓČČ“Ł½ųFe3+Ė®½ā |
·ÖĪö A£®ĀČ»Æļ§ČÜŅŗÖŠļ§øłĄė×ÓĖ®½āĻŌĖįŠŌ£¬Ė®½āĘ½ŗā³£Źż²»±ä£»
B£®Ģ¼ĖįÄĘČÜŅŗÖŠĢ¼ĖįøłĄė×ÓĖ®½āČÜŅŗĻŌ¼īŠŌ£¬Ė®½ā·“Ó¦ĪŖĪüČČ·“Ó¦£¬¼ÓČČ“Ł½ųĖ®½ā£»
C£®“×ĖįĪŖČõĖįČÜŅŗÖŠ“ęŌŚµēĄėĘ½ŗā£¬Ļ”ŹĶČÜŅŗ“Ł½ųµēĄėĘ½ŗāÕżĻņ½ųŠŠ£¬Ę½ŗāדĢ¬ĻĀµÄĄė×ÓÅØ¶Č¼õŠ”£¬ČÜŅŗÖŠ“ęŌŚĄė×Ó»ż³£Źż£»
D£®¼ÓČČ“Ł½ųĮĖµÄFe3+Ė®½ā£»
½ā“š ½ā£ŗA£®³£ĪĀĻĀ£®NH4ClČÜŅŗÖŠ“ęŌŚĖ®½āĘ½ŗā£¬NH4++H2O?NH3•H2O+H+£¬¼ÓĖ®Ļ”ŹĶ“Ł½ųĖ®½ā£¬µŖĖ®½āĘ½ŗā³£Źż²»±ä£¬$\frac{c£ØN{H}_{3}•{H}_{2}O£©c£Ø{H}^{+}£©}{c£ØN{{H}_{4}}^{+}£©}$²»±ä£¬¹ŹA“ķĪó£»
B£®Ģ¼ĖįÄĘČÜŅŗÖŠĢ¼ĖįøłĄė×ÓĖ®½āČÜŅŗĻŌ¼īŠŌ£¬CO32-+H2O?HCO3-+OH-£¬¼ÓČČ“Ł½ųĖ®½āĘ½ŗāÕżĻņ½ųŠŠ£¬ČÜŅŗ¼īŠŌŌöĒ棬PHŌö“󣬹ŹB“ķĪó£»
C£®CH3COOHČÜŅŗ¼ÓĖ®Ļ”ŹĶČÜŅŗµÄµ¼µēÄÜĮ¦¼õČõ£¬Ņņ“ĖČÜŅŗÖŠĘ½ŗāדĢ¬ĻĀĄė×ÓÅØ¶Č¾ł¼õŠ”£¬ČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČŌö“󣬹ŹC“ķĪó£»
D£®Ļņ·ŠĖ®ÖŠµĪ¼ÓFeCl3±„ŗĶČÜŅŗÖĘø÷Fe£ØOH£©3½ŗĢåµÄŌŅņŹĒ¼ÓČČ“Ł½ųµÄFe3+Ė®½ā£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģā擳öĄ“ŃĪĄąĖ®½ā”¢Čõµē½āÖŹµēĄėĘ½ŗā”¢Ó°ĻģĘ½ŗāדĢ¬µÄŅņĖŲ·ÖĪöÅŠ¶Ļ£¬×¢ŅāĘ½ŗā³£ŹżŗĶĄė×Ó»ż³£ŹżµÄ·ÖĪö£¬ÕĘĪÕ»ł“”ŹĒ½āĢāµÄ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ½šŹōµ„ÖŹŌŚ·“Ó¦ÖŠÖ»×÷»¹Ō¼Į | |
| B£® | ·Ē½šŹōµ„ÖŹŌŚ·“Ó¦ÖŠÖ»×÷Ńõ»Æ¼Į | |
| C£® | ½šŹōŹ§µē×ÓŌ½¶ą£¬Ę仹ŌŠŌŌ½ĒæÓŠĮ¦ | |
| D£® | Cu2+±ČFe2+Ńõ»ÆŠŌĒ棬Fe±ČCu»¹ŌŠŌĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | g/L | B£® | % | C£® | mol•L-1 | D£® | L/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 140”ꏱ£¬ĪŽĖ®ŅŅ“¼ÓėÅØĮņĖį¹²ČČæÉÖʱøŅŅĻ© | |
| B£® | ĶłÓĶÖ¬ÖŠ¼ÓĻ”ĮņĖįÓėÖ®¹²ČČæÉ·¢ÉśŌķ»Æ·“Ó¦ | |
| C£® | æÉÓƵāČÜŅŗ¼ģŃéµķ·ŪŹĒ·ńĖ®½āĶźČ« | |
| D£® | ŃéÖ¤äåŅŅĶéÖŠµÄäåŌŖĖŲ£¬æÉÖ±½Ó¼ÓAgNO3ČÜŅŗ¹Ū²ģŹĒ·ńÓŠµ»ĘÉ«³ĮµķÉś³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ź§Č„µē×ӵķ“Ó¦ŹĒ»¹Ō·“Ó¦ | B£® | ·¢ÉśŃõ»Æ·“Ó¦µÄŹĒŃõ»Æ¼Į | ||
| C£® | ×÷Ńõ»Æ¼ĮµÄĪļÖŹ²»ÄÜĶ¬Ź±×÷»¹Ō¼Į | D£® | Ź§Č„µē×ÓµÄĪļÖŹŹĒ»¹Ō¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaHCO3+HClØTNaCl+H2O+CO2”ü | B£® | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{”÷}$ 2KCl+2O2”ü | ||
| C£® | S+O2$\frac{\underline{\;µćČ¼\;}}{\;}$SO2 | D£® | 2CuO+C$\frac{\underline{\;\;”÷\;\;}}{\;}$2Cu+CO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1L 0.1mol/LµÄ°±Ė®ÖŠÓŠ0.1NAøöNH4+ | |
| B£® | ±ź×¼×“æöĻĀ£¬22.4LŃĪĖįŗ¬ÓŠNAøöHCI·Ö×Ó | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬14gÓÉN2ÓėCOµÄ»ģŗĻĘųĢåŗ¬ÓŠ0.5NAøöŌ×Ó | |
| D£® | ±ź×¼×“æöĻĀ£¬6.72L N02ÓėĖ®³ä·Ö·“Ó¦×ŖŅĘ0.2NAøöµē×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
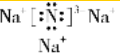 £¬øĆ»ÆŗĻĪļŹĒÓÉĄė×Ó¼üŠĪ³ÉµÄ£®
£¬øĆ»ÆŗĻĪļŹĒÓÉĄė×Ó¼üŠĪ³ÉµÄ£®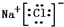 ”¢
”¢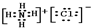 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com