
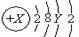 。则X、Y及该原子3p能级上的电子数分别为( )
。则X、Y及该原子3p能级上的电子数分别为( )| A.18、6、4 | B.20、8、6 | C.18、8、6 | D.15~20、3~8、1~6 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
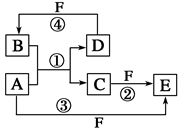
科目:高中化学 来源:不详 题型:单选题
| A.X+ | B.X2+ | C.X3+ | D.X4+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素代号 | I1 | I2 | I3 | I4 |
| E | 500 | 4600 | 6900 | 9500 |
| F | 740 | 1500 | 7700 | 10500 |
| H | 580 | 1800 | 2700 | 11600 |
| I | 420 | 3100 | 4400 | 5900 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.能量守恒原理 |
| B.近似能级图中的顺序 3d 轨道能量比 4s 轨道高 |
| C.洪特规则 |
| D.泡利不相容原理 |
查看答案和解析>>
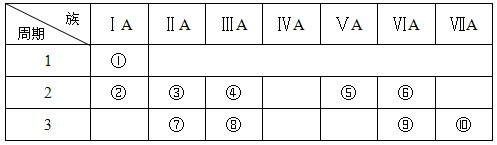
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2CA3(g)
2CA3(g) .0 L.
.0 L.查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com