
£Ø14·Ö£©»ĘĶæó( CuFeS2)ŹĒÖĘČ”Ķ¼°Ęä»ÆŗĻĪļµÄÖ÷ŅŖŌĮĻÖ®Ņ»£¬»¹æÉŅŌÖʱøĮņ¼°ĢśµÄ»ÆŗĻĪļ”£
£Ø1£©”¢ČōŅ±Į¶ĶµÄ·“Ó¦ĪŖ£ŗ8 CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
CuFeS2ÖŠFeµÄ»ÆŗĻ¼ŪĪŖ+2£¬·“Ó¦ÖŠ±»Ńõ»ÆµÄŌŖĖŲŹĒ___________£ØĢīŌŖĖŲ·ūŗÅ£©”£
£Ø2£©”¢ÉĻŹöŅ±Į¶¹ż³ĢÖŠ²śÉś“óĮæSO2£¬ĻĀĮŠ“¦Ąķ·½°øŗĻĄķµÄŹĒ___________£ØĢī“śŗÅ£©”£
a£®øßæÕÅÅ·Å b£®ÓĆÓŚÖʱøĮņĖį
c£®ÓĆÅØĮņĖįĪüŹÕ d£®ÓĆ“æ¼īČÜŅŗĪüŹÕÖĘNa2SO3
£Ø3£©”¢²ÉÓĆ»š·ØČŪĮ¶¹¤ŅÕÉś²śĶµÄÖŠ¼ä¹ż³Ģ»į·¢ÉśCu2OÓėCu2SŌŚøßĪĀĻĀ×Ŗ»ÆĪŖCu£¬·Å³öSO2ĘųĢåµÄ·“Ó¦”£ČōCu2OŗĶCu2SÕżŗĆĶźČ«·“Ó¦£¬Cu2OŗĶCu2SµÄĪļÖŹµÄĮæÖ®±ČĪŖ_____£»Cu2SŗĶHNO3ÓŠČēĻĀ·“Ó¦£ŗ3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO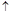 +8H2OČōÉś³É11.2LNO(±ź×¼×“æö)£¬Ōņ·“Ó¦ÖŠ×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ__________”£
+8H2OČōÉś³É11.2LNO(±ź×¼×“æö)£¬Ōņ·“Ó¦ÖŠ×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ__________”£
£Ø4£©”¢¹ż¶žĮņĖį¼Ų(K2S2O8)¾ßÓŠĒæŃõ»ÆŠŌ£¬æɽ«I”ŖŃõ»ÆĪŖI2£ŗS2O82£+2I”Ŗ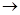 2SO42£+I2Ķعżøı䷓ӦĶ¾¾¶£¬Fe3+”¢Fe2+¾łæÉ“ß»ÆÉĻŹö·“Ó¦”£ŹŌÓĆĄė×Ó·½³ĢŹ½±ķŹ¾Fe2+¶ŌÉĻŹö·“Ó¦µÄ“߻ƹż³Ģ£ŗ____________________________”¢______________________________”£
2SO42£+I2Ķعżøı䷓ӦĶ¾¾¶£¬Fe3+”¢Fe2+¾łæÉ“ß»ÆÉĻŹö·“Ó¦”£ŹŌÓĆĄė×Ó·½³ĢŹ½±ķŹ¾Fe2+¶ŌÉĻŹö·“Ó¦µÄ“߻ƹż³Ģ£ŗ____________________________”¢______________________________”£
 æģ½ŻÓ¢ÓļÖÜÖÜĮ·ĻµĮŠ“š°ø
æģ½ŻÓ¢ÓļÖÜÖÜĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
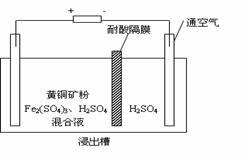 £Ø8·Ö£©ŅŌŹÆÄ«ĪŖµē¼«£¬µē½ā·Ø“¦Ąķ»ĘĶæó£ØCuFeS2£©¾«æó£¬æÉŅŌÖʵĆĮņĖįĶČÜŅŗŗĶµ„ÖŹĮņ”£»ĘĶæóŌŚŃō¼«µÄ½ž³ö·“Ó¦±Č½Ļø“ŌÓ£¬Ö÷ŅŖÓŠ£ŗ
£Ø8·Ö£©ŅŌŹÆÄ«ĪŖµē¼«£¬µē½ā·Ø“¦Ąķ»ĘĶæó£ØCuFeS2£©¾«æó£¬æÉŅŌÖʵĆĮņĖįĶČÜŅŗŗĶµ„ÖŹĮņ”£»ĘĶæóŌŚŃō¼«µÄ½ž³ö·“Ó¦±Č½Ļø“ŌÓ£¬Ö÷ŅŖÓŠ£ŗ
CuFeS2 + 4H+ = Cu2+ + Fe2+ + 2H2S£¬
CuFeS2 + 4Fe3+ = Cu2+ + 5Fe2+ + 2S£¬
2Fe3+ + H2S = 2H+ + S”ż + 2Fe2+”£ÓŅĶ¼ĪŖøĆ¹¤ŅÕµÄŹ¾ŅāĶ¼”£
£Ø1£©µē½ā¹ż³ĢŹµĻÖĮĖFe3+µÄŃ»·£¬ŌņŃō¼«·½³ĢŹ½ĪŖ ”ų ”£
£Ø2£©µē½ā¹ż³ĢÖŠŅõ¼«Īö³öµÄ½šŹōĪŖ ”ų £¬ĻņŅõ¼«ĶØæÕĘųµÄŌŅņŹĒ ”ų ”£
£Ø3£©ÓėČ¼ÉÕ·ØĮ¶ĶĻą±Č£¬µē½ā·ØµÄÓŵćĪŖ ”ų ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com