
| A. | 稳定性:H2S>HF | B. | HCl的电子式: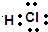 | ||
| C. | 在卤化氢中HI最稳定 | D. | 沸点:PH3>NH3 |
分析 A.非金属性越强,对应氢化物的稳定性越强;
B.氯化氢为共价化合物,分子中含有1个H-C键;
C.非金属性越强,氢化物的稳定性越强;
D.氨气分子中含有氢键,导致其沸点较高.
解答 解:A.非金属性F>S,则气态氢化物的稳定性:H2S<HF,故A错误;
B.HCl为共价化合物,Cl原子最外层达到8电子稳定结构,其电子式为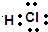 故B正确;
故B正确;
C.卤素元素中,原子序数越大,非金属性越弱,非金属性最强的为F,则在卤化氢中HF最稳定,故C错误;
D.NH3分子中含有氢键,大大增加了分子间作用力,则沸点:PH3<NH3,故D错误;
故选B.
点评 本题考查了原子结构与元素周期律的应用,题目难度不大,明确元素周期律内容为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的灵活应用能力.


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源:2016-2017学年四川省高一上第一次月考化学卷(解析版) 题型:选择题
从1 L 1 mol/L NaOH溶液中取出100 mL,下列关于这100 mL溶液的叙述中错误的是 ( )
A.含NaOH 0.1 mol B.c(Na+)浓度为0.1 mol/L
C.含NaOH 4 g D.c(OH-)浓度为 1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3遇少量酸可转化为NaHCO3 | |
| B. | 在水中的溶解度Na2CO3比NaHCO3大 | |
| C. | 与同浓度的硫酸反应时,Na2CO3比NaHCO3剧烈 | |
| D. | NaHCO3比Na2CO3的碱性弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 |  |  |  |
| 图Ⅰ碱性锌锰电池 | 图Ⅱ铅硫酸蓄电池 | 图Ⅲ电解精炼铜 | 图Ⅳ银锌纽扣电池 |
| A. | 图Ⅰ所示装置中,MnO2是正极,工作时其还原产物是MnOOH | |
| B. | 图Ⅱ所示装置充电过程中,阴极的电极反应式为PbSO4(s)+2e-=Pb(s)+SO42-(aq) | |
| C. | 图Ⅲ所示装置工作过程中,电解质溶液中Cu2+ 浓度始终不变 | |
| D. | 图Ⅳ所示电池中,工作时OH-移向锌电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
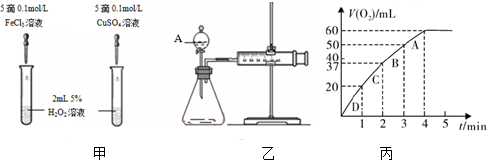
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 白醋中滴入石蕊试液呈红色 | B. | 白醋中c(H+)=0.01 moL/L | ||
| C. | 蛋壳浸泡在白醋中有气体放出 | D. | 白醋加入豆浆中有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com