
用标准的NaOH溶液滴定未知浓度的盐酸,若测定结果偏低,其原因可能是( )
A. 滴定终点读数时,俯视滴定管的刻度,其他操作正确
B. 配制标准溶液的固体NaOH中混有杂质KOH
C. 盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D. 滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
科目:高中化学 来源:辽宁省大连市2017届高三3月双基测试化学试卷 题型:简答题
CO和H2均是重要的化工原料,CO2的固定和利用对环境保护及能源开发具有重要的意义。
(1)利用水煤气(CO+H2)作为合成气,在同一容器中,选择双催化剂,经过如下三步反应,最终合成二甲醚(CH3OCH3)。
甲醇合成反应:CO(g)+2H2(g) CH3OH(g) △H1=-90.8kJ·mol-1
CH3OH(g) △H1=-90.8kJ·mol-1
水煤气变换反应:CO(g)+H2O(g) CO2(g)+H2(g) △H2=-41.3kJ·mol-1
CO2(g)+H2(g) △H2=-41.3kJ·mol-1
甲醇脱水反应:2CH3OH(g) CH3OCH3(g)+H2O(g) △H3=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H3=-23.5kJ·mol-1
写出由CO和H2合成二甲醚气体和水蒸气的热化学方程式____________。
(2)在2L恒容密闭容器中,投入CO(g)和H2(g)各5mol,发生如下反应:
3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) △H<0,CO的转化率α与温度、压强的关系如图所示:
CH3OCH3(g)+CO2(g) △H<0,CO的转化率α与温度、压强的关系如图所示:
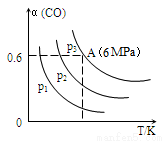
①p1、p2、p3中最大的是________。
②若该反应进行50min时达到平衡,此时CO的转化率α=0.6,则50min内H2的反应速率为____mol·L-1·min-1。
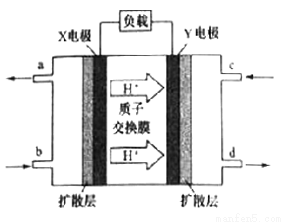
(3)二甲醚(CH3OCH3)燃料电池具有启动快。效率高等优点,其能量密度高于甲醇燃料电池。其工作原理如图所示。X极附近的酸性______(填“减弱”、“增强”或“不变”),Y电极是_____极,写出X电极上发生的电极反应式__________。若用该二甲醚燃料电池电解饱和食盐水(阳极为石墨电极),当有2.3g燃料被消耗时,阴极产生气体的体积为_____L(标准状况下)
查看答案和解析>>
科目:高中化学 来源:2017届贵州省贵阳市高三2月适应性考试(一)理综化学试卷(解析版) 题型:选择题
锂一二硫化亚铁电池是一种高容量电池,用途广泛,该电池放电时的总反应为:4Li+FeS2=Fe+2Li2S。下列说法正确的是
A. 放电时,负极反应为:Li-e-=Li+
B. 放电时,正极发生氧化反应
C. 硫酸、羧酸及醇类物质都可以用作该锂电池的电解质
D. 充电时,阳极只有Fe参与放电
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省长沙市高二上学期期末考试化学试卷(解析版) 题型:推断题
已知:醛(或酮)在一定条件下(稀NaOH溶液中)可以两分子加成得到β-羟基醛(或酮),后者微热脱水生成α、β不饱和醛(或酮)。
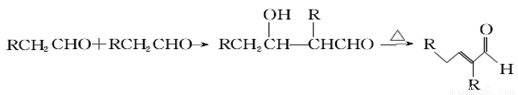
聚合物F的合成路线图如下:
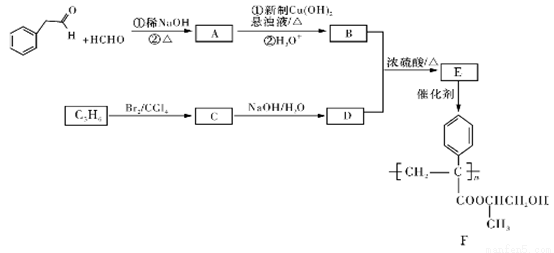
请据此回答:
(1)A中含氧官能团名称是_________。
(2)E→F的反应类型是____________。
(3)写出下列反应的化学方程式:
A→B的反应①__________________________;
C→D:____________________________;
(4)已知同一个碳原子上连两个碳碳双键的结构不稳定,如果C与NaOH的醇溶液反应,则生成的有机物的结构简式为_______________。
(5)G物质与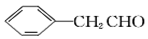 互为同系物,且G物质的相对分子质量比
互为同系物,且G物质的相对分子质量比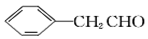 大14,则符合下列条件的G的同分异构体有________种。
大14,则符合下列条件的G的同分异构体有________种。
① 分子中含有苯环,且苯环上有两个取代基
② 遇氯化铁溶液变紫色
③ 能与溴水发生加成反应
(6)参照上述合成路线,设计一条由甲醛、丙醛和甲醇为有机原料(除溶剂外不得使用其它有机物)合成有机玻璃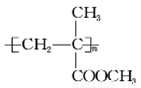 的合成路线。____________
的合成路线。____________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省长沙市高二上学期期末考试化学试卷(解析版) 题型:选择题
如下流程中a、b、c、d、e、f是六种有机物,其中a是烃类,其余是烃的衍生物。下列有关说法正确的是
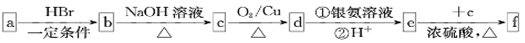
A. 若a的相对分子质量是42,则d是乙醛
B. 若d的相对分子质量是44,则a是乙炔
C. 若a为苯乙烯(C6H5-CH=CH2),则f的分子式是C16H32O2
D. 若a为单烯烃,则d与f的最简式可能相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省长沙市高二上学期期末考试化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数,下列说法正确的是( )
A. 标准状况下,22.4LCH4和CH2Cl2的混合物所含有的分子数目为NA
B. 3g的甲基中含有的电子数为1.6NA
C. 0.5mol的有机物C15H32中含有的共键数为24NA
D. 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA
查看答案和解析>>
科目:高中化学 来源:广东省2016-2017学年高一上学期期末考试化学试卷 题型:填空题
实验室里通常用MnO2与浓盐酸反应制取氯气,其反应的化学方程式为:MnO2 + 4HCl(浓) 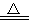 MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
(1)用单线桥法表示该反应电子转移的方向和数目:___________。
(2)在该反应中,如有1 mol Cl2生成,被氧化的HCl的物质的量是___________,转移电子的数目是_____________。
(3)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与ClO3-物质的量之比为1∶1的混合液,反应的化学方程式是 _________________________ 。
(4)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)_________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省台州市高一上学期期末质量评估考试化学试卷(解析版) 题型:填空题
A、B、C均为中学化学常见的纯净物,它们之间存在如下转化关系,其中①②③均为有单质参与的反应。
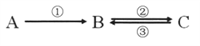
(1)若A是常见的金属,①③中均有同一种气态非金属单质参与反应,B溶液遇KSCN显血红色,且②为化合反应,写出反应②的离子方程式________。
(2)若B是太阳能电池用的光伏材料,①②③为工业制备B的反应。C的化学式是______,写出反应①的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高二下学期开学考试化学试卷(解析版) 题型:填空题
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。T℃时反应
2SO2(g)+O2(g) 2SO3(g)过程中的能量变化如图所示,回答下列问题。
2SO3(g)过程中的能量变化如图所示,回答下列问题。
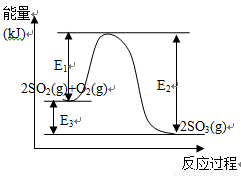
(1)T℃时将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。2min时反应达到平衡,此时测得反应物O2还剩余0.1mol,则达到平衡时SO2的转化率为_______,反应放出_____________热量。(用E1、E2或E3表示)
(2)下列叙述能证明该反应已达化学平衡状态的是__________________(填序号)
①SO2的体积分数不再发生变化 ②容器内压强不再发生变化 ③容器内气体原子总数不再发生变化 ④相同时间内消耗2n molSO2的同时生成n molO2 ⑤相同时间内消耗2n molSO2的同时生成2n molSO3
(3)在反应体系中加入催化剂,反应速率增大, E3的变化是: E3 ____________(填“增大”“减小”或“不变”)
(4)若以下图所示装置,用电化学原理生产硫酸,将SO2、O2以一定压强喷到活性电极上反应。写出通SO2电极的电极反应式:______________________________________________。
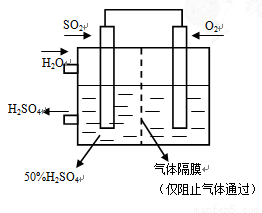
(5) SOCl2是一种无色液体,可与碳共同构成锂电池的正极材料,且其放电时也有SO2气体产生。写出SOCl2在电池中放电时的电极反应式_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com