
在一定温度下,在1L容器中,a mol SO2与b mol O2反应2SO2+O2⇌2SO3达到平衡时有c mol SO2发生了反应,则:
(1)生成 mol SO3;
(2)O2的转化率为
(3)平衡时容器内气体总物质的量为 ()mol
(4)平衡体系中SO3的百分含量(体积比) ×100%
(5)平衡浓度[SO2]= mol•L﹣1.
考点:
化学平衡的计算.
专题:
化学平衡专题.
分析:
依据化学平衡三段式列式计算
2SO2+O2⇌2SO3
起始量(mol) a b 0
变化量(mol) c 0.5c c
平衡量(mol) a﹣c b﹣0.5c c
据此分析计算.
解答:
解:依据化学平衡三段式列式计算
2SO2+O2⇌2SO3
起始量(mol) a b 0
变化量(mol) c 0.5c c
平衡量(mol) a﹣c b﹣0.5c c
(1)计算可知,反应生成三氧化硫物质的量为cmol;
故答案为:c;
(2)O2的转化率=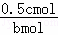 ×100%=
×100%=
故答案为: ;
;
(3)平衡时容器内气体总物质的量=a﹣c+b﹣0.5c+c=(a+b﹣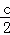 )mol;
)mol;
故答案为:(a+b﹣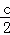 )mol;
)mol;
(4)平衡体系中SO3的百分含量= ×100%=
×100%= ×100%;
×100%;
故答案为: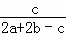 ×100%;
×100%;
(5)平衡浓度[SO2]=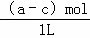 =(a﹣c)mol/L;
=(a﹣c)mol/L;
故答案为:a﹣c.
点评:
本题考查了化学平衡计算应用,主要是转化率、含量、浓度的计算分析应用,掌握基础是关键,题目难度中等.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
下列有关原子结构和元素周期律的表述正确的是( )
①原子序数为15的元素的最高化合价为+3;
②ⅦA族元素是同周期中非金属性最强的元素;
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6;
④原子序数为12的元素位于元素周期表的第三周期ⅡA族.
A. ①② B. ①③ C. ②④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
“5•12”地震给四川等省市人民群众带来巨大的灾难.在灾区经常发生因混合使用消毒剂或洁污剂而产生的氯气中毒事件,据此推测,产生类似中毒事件的相混合的洁污剂或消毒剂中最有可能含有的离子或物质是( )
A. ClO3﹣,Cl﹣,K+ B. ClO﹣,Cl﹣,H+
C. NaClO,NaClO3,NaNO3 D. NaClO,Na2SO4,NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应达到平衡后增大压强或降低温度,平衡都向正反应方向移动的是( )
|
| A. | 2NO2(g)⇌N2O4(g);△H<0 | B. | 3O2(g)⇌2O3(g);△H>0 |
|
| C. | H2(g)+I2(g)⇌2HI(g);△H<0 | D. | 2NH3(g)⇌3H2(g)+N2(g);△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,发生CO+NO2⇌CO2+NO的反应,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的说法中正确的是( )
|
| A. | 正反应为吸热反应 | B. | 正反应为放热反应 |
|
| C. | 降温后CO的浓度增大 | D. | 降温后各物质的浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在5L物质的量浓度为2mol/l的K2SO4溶液中K+的物质的量浓度为 ( )
A.2mol/l B.4mol/l C.1 mol/l D.20mol/l
查看答案和解析>>
科目:高中化学 来源: 题型:
欲配制100ml 1.0 mol/L Na2SO4溶液,正确的方法是 ( )
①将32.2g Na2SO4·10H2O溶于少量水中,再用水稀释至100 ml
② 将14.2 g Na2SO4 溶于100ml水中制成溶液
③ 将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 ml
A.①② B.①②③
C.①③ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
从植物花汁中提取的一种有机物,可简化表示为HIn,在水溶液中因存在下列平衡,故可用作酸、碱指示剂:
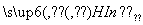 H+(溶液)+
H+(溶液)+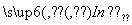
在上述溶液中加入下列物质,最终能使指示剂显黄色的是( )
A.盐酸 B.NaHCO3溶液
C.NaHSO4溶液 D.Na2O2(固体)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 浓硫酸的腐蚀性不是化学变化
B. 可以通过化学反应完成16O到18O的转变
C. 胶体的聚沉属于物理变化
D. 焰色反应一定发生化学变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com