
【题目】0.1 mol某烃完全燃烧生成0.4 mol H2O,生成CO2为0.8mol,则此有机物的分子式为______。若它是能聚合成高分子化合物的芳香族化合物,其结构简式为______;若其不能与氢气发生加成反应,则为__________,(提示立体结构)它的二氯代物有_______种。
科目:高中化学 来源: 题型:
【题目】Ⅰ、下图是维生素A的分子结构:
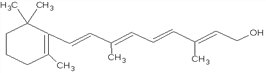
(1)维生素A的分子式是__________________,1mol维生素A最多能与____________mol溴发生加成反应。
(2)根据要求写出下列有机物的结构简式或者系统命名:
CH3CH(CH3)C(CH3)2CH2CH3 :__________________________________.
2﹣甲基﹣2﹣丁烯:________________________________________________.
Ⅱ、人们对苯及芳香烃的认识有一个不断深化的过程。
(3)已知分子式为C6H6的结构有多种,其中的两种见图(Ⅰ)、(Ⅱ):
![]()
①这两种结构的区别表现在:
定性方面(即化学性质方面):Ⅰ不能_______(填字母,下同)而Ⅱ不能________.
A.被酸性高锰酸钾溶液氧化 B.与溴的四氯化碳溶液发生加成反应
C.与溴在催化剂作用下发生取代反应 D.与氢气发生加成反应
定量方面:1molC6H6与H2加成时:Ⅰ需________mol,而Ⅱ需_______mol.
②今发现C6H6还有另一种如图立体结构![]() :该结构的二氯代物有________种.
:该结构的二氯代物有________种.
③根据苯的分子结构,可以推测苯的性质比较稳定,容易发生取代反应,不易发生加成和氧化反应。写出苯与硝酸在催化剂作用下反应的化学方程式____________________________
(4)已知萘的结构简式为 ![]() ,下列关于萘的说法正确的是_______(填编号)
,下列关于萘的说法正确的是_______(填编号)
A.萘的分子式为C10H10 B.1mol萘能与6molH2发生加成反应
C.萘分子中所有原子在同一平面上 D.一溴代萘只有两种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1L0.1mol/LNH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3·H2O的变化趋势如右图所示(不考虑体积变化和氨的挥发)。下列说法不正确的是

A. M点溶液中水的电离程度比原溶液小
B. 在M点时,n(OH-)-n(H+)=(a-0.05)mol
C. 随着NaOH的加入,  不断增大
不断增大
D. 当n(Na0H)=0.1mol时,c(Na+)=c(NH4+)+c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的离子能在溶液中大量共存的是( )
A. Na+、Mg2+、Cl-、NO3- B. SO42-、Fe2+、K+、OH-
C. Ba2+、Cu2+、SO42-、Cl- D. HCO3-、CO32-、K+、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“保护环境,就是保护自己”。目前,在我国城市环境中主要的大气污染物是( )
A、SO2、NO、CO、烟尘 B、CO2、Cl2、N2、酸雨
C、HCl、SO2、N2、粉尘 D、CO2、NO、NH3、雾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表所列各组物质中,物质之间通过一步反应不能实砚如下图所示转化的是
选项 | X | Y | Z |
A | Na | NaOH | NaCl |
B | Si | SiO2 | Na2SiO3 |
C | Cl2 | HClO | NaClO |
D | NO | NO2 | HNO3 |

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有反应N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0,
2NH3(g) ΔH<0,
(1)在恒温恒压条件下进行,反应正向进行的是________;反应逆向进行的是________;处于平衡状态的是________;无法判断是否达到平衡的是________。
A.单位时间内生成1mol N2,同时生成3mol NH3
B.单位时间内生成3mol N2,同时生成6mol N—H键
C.混合气体的密度不再随时间而改变
D.容器中气体的压强不再随时间而改变
(2)在一定温度下某恒容密闭容器中,充入3molH2和1mol的N2,2min达到平衡状态时,总的气体的物质的量变为原来的9/10,则此时N2的转化率为__________;
若此时放出的热量为18.44 kJ,则其热化学方程式为______________________________ .
根据所求出的热化学方程式,且已知1mol氮氮三键断裂需要为945.8kJ的能量,1mol氢氢键断裂需要436 kJ的能量,求1molN-H键断裂吸收的能量_____。
(3)氨气可用作碱性燃料电池的燃料,电池反应为4NH3+3O2═2N2+6H2O,
则氨燃料电池的负极电极反应为________________________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com