
【题目】已知钠、铁都能与水反应,下列叙述不正确的是( )
A.它们反应的难易程度不同B.它们反应的产物不完全相同
C.都需在高温条件下进行D.反应类型都是置换反应
【答案】C
【解析】
A.根据钠、铁与水反应的剧烈程度判断;
B.根据二者反应产物分析;
C.结合二者反应的条件判断;
D.根据置换反应的概念分析。
A.Na在室温下与冷水会剧烈反应,而炽热的铁在高温条件下,与水蒸气发生反应,可见Na与水反应要比铁剧烈得多,A正确;
B.Na在室温下与冷水反应产生NaOH、H2;炽热的Fe与水蒸气在高温条件下反应产生Fe3O4、H2,可见产物不完全相同,B正确;
C.Na与水反应在室温下发生剧烈反应,不需要高温条件,C错误;
D.Na与H2O反应方程式为2Na+2H2O=2NaOH+H2↑;Fe与水蒸气反应的方程式为3Fe+4H2O(g)![]() Fe3O4+4H2,二者都是单质与化合物反应产生新的单质和新的化合物,因此反应类型都属于置换反应,D正确;
Fe3O4+4H2,二者都是单质与化合物反应产生新的单质和新的化合物,因此反应类型都属于置换反应,D正确;
故合理选项是B。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】现有14.4 g CO和CO2的混合气体,在标准状况下,其体积为8.96 L。回答下列问题:
(1)该混合气体的平均摩尔质量为________________。
(2)混合气体中碳原子的个数为______________(用NA表示阿伏加德罗常数的值)。
(3)将混合气体依次通过如图所示装置,剩余气体最后收集在气球中(实验在标准状况下测定)。
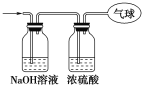
①气球中收集到的气体中,电子总数为________(用NA表示阿伏加德罗常数的值)。
②气球的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关描述不正确的是
A.新制饱和氯水和浓硝酸光照下均会有气体产生,其成分中都有氧气
B.灼烧NaOH固体时不能使用瓷坩埚,因为瓷坩埚中的SiO2能与NaOH反应
C.钠在空气和氯气中燃烧,火焰皆呈黄色,但生成固体颜色不同
D.浓硫酸具有较强酸性,能与Cu反应生成H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为主要原料合成一种具有果香味有机物C和高分子化合物E的合成路线如图1所示。
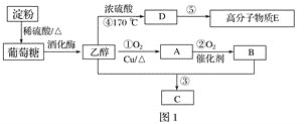
请回答下列问题:
(1)E的结构简式为________,D分子内含有的官能团是________(填名称)。
(2)写出反应②的反应类型:________。
(3)写出下列反应的化学方程式:
①________________________________________________________________________;
③________________________________________________________________________。
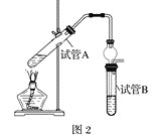
(4)某同学欲用图2装置制备物质C,试管B中装有足量的饱和碳酸钠溶液的目的是:________________________________________;插入试管B的导管接有一个球状物,其作用为________________________________________________________________________;如需将试管B中的物质C分离出来,用到的主要玻璃仪器有:烧杯、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是
A.用铁电极电解饱和食盐水:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
B.Fe(NO3)3溶液中加入过量的HI溶液2Fe3++2I-=2Fe2++I2
C.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
D.向Mg(HCO3)2溶液中加入过量的NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+5B(g)![]() 4C(g)+6D(g),在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.30 mol。下列叙述正确的是( )
4C(g)+6D(g),在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.30 mol。下列叙述正确的是( )
A. A的平均反应速率是0.010 molL﹣1s﹣1
B. 容器中含D物质的量至少为0.45 mol
C. 容器中A、B、C、D的物质的量的比一定是4∶5∶4∶6
D. 容器中A的物质的量一定增加了0.30 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸镍(NiSO4)是一种重要的化工原料,广泛应用于电镀、医药、印染等工业。以含镍废催化剂(主要含Ni及少量的Al、Al2O3、Fe和其它不溶于酸、碱的杂质)为原料生产NiSO4·7H2O晶体的两种工艺流程如下:
流程一:
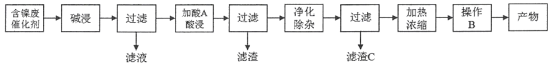
流程二:
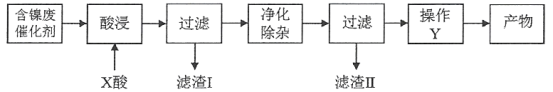
已知:部分金属氢氧化物的Ksp近似值如下表所示:
化学式 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp近似值 | 10-17 | 10-39 | 10-34 | 10-15 |
回答下列问题:
(1)流程一中所用酸A和流程二中所用酸X___________(填“相同”或“不相同”);流程一中滤渣C和流程二中滤渣II___________(填“相同”或“不相同”)。流程二中滤渣I是___________。
(2)流程一中“碱浸”时发生反应的离子方程式为_________________、___________________。
(3)流程二中“净化除杂”包含了两步操作过程:第一步,加入氧化剂H2O2,发生反应的离子方程式是____________________________________________;第二步,调节溶液的pH。
(4)分析比较流程一中操作B和流程二中操作Y后,回答操作Y是___________、___________、过滤、洗涤、干燥,即得产物。
(5)由己知信息列式计算:常温下,Ni2+完全沉淀时的pH值___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本反应类型的关系如下图,则下列化学反应属于区域3的是

A.IBr + H2O == HIO + HBr
B.2NaHCO3![]() Na2CO3 + H2O + CO2↑
Na2CO3 + H2O + CO2↑
C.Fe3O4 + 4CO ![]() 3Fe + 4CO2
3Fe + 4CO2
D.Zn + H2SO4 == ZnSO4 + H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计及其对应的离子方程式均正确的是( )
A. 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+
B. Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑
C. 将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl-+ClO-
D. 明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com